
科目: 来源: 题型:
将氨水滴加到盛有AgCl浊液的试管中,AgCl逐渐溶解,再加入NaBr溶液又产生了浅
黄色沉淀。对上述过程,下列理解或解释中正确的是
A.Ksp(AgCl)<Ksp(AgBr) B.上述实验说明AgCl没有NaBr稳定
C.氨水破坏了AgCl的溶解平衡,NaBr又破坏了银氨络离子的电离平衡
D.若在AgCl浊液中直接加入NaBr溶液,也会产生浅黄色沉淀
查看答案和解析>>
科目: 来源: 题型:
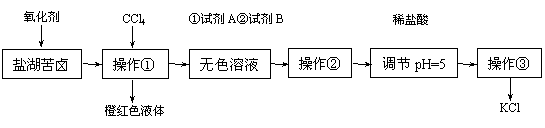 (12分)某研究性学习小组拟提纯粗盐并取苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程:
(12分)某研究性学习小组拟提纯粗盐并取苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程:
请根据上述流程,回答以下问题:
⑴要从橙红色液体中分离出溴,可采取的操作是 。
⑵试剂A中有两种溶质,它们是 ,试剂B成分是 。(填化学式)
⑶检验SO42-已除尽的方法是_________________________________________。
⑷用盐酸调节溶液的pH至pH=5的目的是 。
⑸控制溶液pH=12可确保Mg2+除尽,此时溶液中Mg2+物质的量浓度为 。
(已知Mg(OH)2的Ksp=1.6×10-11)
查看答案和解析>>
科目: 来源: 题型:
(8分)现有药品:①蒸馏水;②AgNO3溶液;③熟石灰;④Na2CO3;⑤稀(NH4)2S溶液;⑥食醋;⑦废干电池(锌筒内填有炭粉、MnO2、NH4Cl、淀粉等糊状物)。某课外小组一准备进行如下实验研究:
⑴利用上述药品制NaOH溶液,化学方程式为 。
⑵在上述基础上制备CO2气体,对应的离子方程式是 。
⑶尝试从废干电池中制备NH4Cl。将废电池中的混合物溶于少量的水中,过滤除去不溶物,再蒸发滤液,并灼烧以制得干燥的NH4Cl晶体。你认为这一设想是否合理(请说明判断理由)? 。
⑷设计实验粗略比较Ag2S与AgCl溶解度大小: 。
查看答案和解析>>
科目: 来源: 题型:
下列化学实验事实及其解释都正确的是
 A. 将饱和氯水滴到淀粉碘化钾试纸上出现如图现象,说明低浓度氯水能将I—氧化成I2,高浓度氯水能将I2进一步氧化成碘的化合物
A. 将饱和氯水滴到淀粉碘化钾试纸上出现如图现象,说明低浓度氯水能将I—氧化成I2,高浓度氯水能将I2进一步氧化成碘的化合物
B. 将过量CO2通入Ca(ClO)2溶液得澄清溶液,说明H2CO3的酸性比HClO弱
C. 用饱和Na2CO3溶液可将BaSO4转化为BaCO3,说明Ksp(BaSO4)>Ksp(BaCO3)
D. 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜熔点高
查看答案和解析>>
科目: 来源: 题型:
下列有关说法中不正确的是
A.工业上可利用海水制取镁
B.实验室可以海带为原料获得碘
C.工业上可通过分离煤焦油获得芳香烃
D.工业上可用氧化剂氧化赤铁矿(含Fe2O3)获得铁
查看答案和解析>>
科目: 来源: 题型:
(10分)S2Cl2是一种金黄色易挥发的液体(熔点:-76℃,沸点:138℃),具有强烈的窒息性,且易与水发生水解反应,生成H2S、SO2、H2SO3、H2SO4等物质。人们使用它作橡胶硫化剂,使橡胶硫化,改变生橡胶热发粘冷变硬的不良性能。
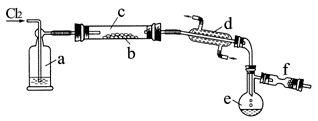
在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
⑴已知S2Cl2分子结构与H2O2相似,请写出S2Cl2的电子式 。
⑵装置a中应放试剂为 ,其作用为 ;装置c水平放置的原因是 ;装置d的名称是 ,它的作用是 。
⑶该实验的操作顺序应为 (用序号表示)。
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2 ⑤停止加热装置c
⑷图中f装置中应放置的试剂为 ,其作用为 。
查看答案和解析>>
科目: 来源: 题型:
从节约原料和防止环境污染因素考虑,用铜制取硝酸铜,方法最佳的是
A.Cu ![]() Cu(NO3)2 B.Cu
Cu(NO3)2 B.Cu ![]() Cu(NO3)2
Cu(NO3)2
C.Cu ![]() CuCl2
CuCl2 ![]() Cu(NO3)2 D.Cu
Cu(NO3)2 D.Cu ![]() CuO
CuO ![]() Cu(NO3)2
Cu(NO3)2
查看答案和解析>>
科目: 来源: 题型:
| 无内容 |
查看答案和解析>>
科目: 来源: 题型:
![]() 1)油脂、淀粉、蛋白质是三种重要的营养成分,其中___________不是高分子化合物,它们都能发生___________反应,淀粉的最终产物是(写化学式) __________,蛋白质的最终产物是_____________,提纯蛋白质可以用的方法是 。
1)油脂、淀粉、蛋白质是三种重要的营养成分,其中___________不是高分子化合物,它们都能发生___________反应,淀粉的最终产物是(写化学式) __________,蛋白质的最终产物是_____________,提纯蛋白质可以用的方法是 。
2)正常雨水PH为 ___________ ,这是因为 的缘故;酸雨是指 的降水,我国主要以 型酸雨为主,是由我国以 为主的能源结构造成的。
3)金属是一种重要的材料,人类的生活和生产都离不开金属,从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限:
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
(1)每年世界上钢铁的产量很高,但钢铁的腐蚀也给人类带来了巨大的损失,铁在潮湿的空气中锈蚀主要属于电化学腐蚀,其负极的电极反应为 ,并写出两种不同类型的防腐的方法 、 。
(2)铝的活动性比铁强,但铝在空气中却比铁表现出良好的抗腐蚀性,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com