
科目: 来源: 题型:
(10分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
 (2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应
负极反应 。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu | ||
查看答案和解析>>
科目: 来源: 题型:
下列现象与电化学腐蚀无关的是
A.黄铜(铜锌合金)制作的铜锣不易生锈 B.银质物品久置变暗
C.铁质器件附有铜质配件,在接触处易生锈 D.生铁比纯铁容易生锈
查看答案和解析>>
科目: 来源: 题型:
(4分)(1)工业上接触法制硫酸的三个主要设备分别是 、接触室、吸收塔。
(2)目前工业上电解饱和食盐水常用的电解槽称为 电解槽。
(3)钢铁在潮湿的空气中发生的腐蚀称为 腐蚀。
(4)工业上从海水中提取金属镁的步骤中不涉及的反应类型是: (从分解反应、化合反应、复分解反应、置换反应中选择一种)。
查看答案和解析>>
科目: 来源: 题型:
(10分)氯化亚铜
不仅在无机化工生产中具有重要作用,在有机合成工业中还可作催化剂。以下是从含Cu2+、Fe3+的电镀废液中制备氯化亚铜的工艺流程图。
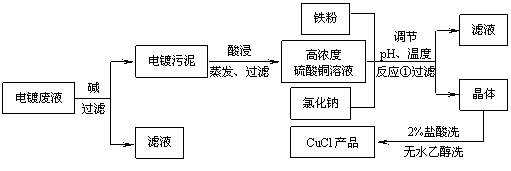 |
下图曲线可表示滤液中金属离子含量与pH、CuCl产率与反应①混合液中pH的关系。
 |
试填空。
(1)当pH=5时,在电镀废液中再加入氢氧化钠溶液生成电镀污泥的离子反应方程式为:
▲ 。
(2)由反应①制备CuCl时的最佳pH在 ▲ 左右。
(3)已知在隔绝空气条件下进行反应①时CuCl产率较高,则CuCl具有 ▲ 的特性。
(4)反应①中1mol铁粉完全反应转移2mol电子,该离子反应的方程式为: ▲ 。
如果将反应①中铁粉换为亚硫酸钠,也可以得到氯化亚铜,则化学方程式为: ▲ 。
查看答案和解析>>
科目: 来源: 题型:
 (12分)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
(12分)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
![]() Pb+PbO2+4H++2SO42- 2PbSO4+2H2O回答下列问题
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O回答下列问题
(1)放电时:负极材料是 ;电解液中H2SO4的浓度将变__ ______,当外电路通过1mol电子时,理论上负极板的质量变化 g。
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成__________,B电极上生成________,此时电解液中H2SO4的浓度将变__ ______。
查看答案和解析>>
科目: 来源: 题型:
![]() 蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁
蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁
标有“+”,另一个接线柱旁标有“—”。关于标有“+”的接线柱,下列说法中正确的是
A.充电时作阳极,放电时作正极 B.充电时作阳极,放电时作负极
C.充电时作阴极,放电时作负极 D.充电时作阴极,放电时作正极
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com