
科目: 来源: 题型:
下列离子方程式书写正确的是
A.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH- = BaSO4↓+H2O
B.NaClO溶液与FeCl2溶液混合:Fe2+ + 2ClO- + 2H2O= Fe(OH)2↓ + 2HClO
C.NH4HSO3溶液与足量NaOH溶液反应:NH4+ + OH-= NH3↑ + H2O
D.将1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积互相均匀混合:
6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+
查看答案和解析>>
科目: 来源: 题型:
(9分)粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量
较多的SiO2(其他成分不含Al和Si)。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3
和NaAlO2,有关化学方程式为:
Al6Si2O13 + 3Na2CO3 = 2NaAlSiO4+ 4NaAlO2 + 3CO2↑ ①
Al6Si2O13 + 5Na2CO3 = 2Na2SiO3 + 6NaAlO2 + 5CO2↑ ②
SiO2 + Na2CO3 = Na2SiO3 + CO2↑ ③
⑴粉煤灰中铝的质量分数为 % (精确到0.1%)
⑵用1 mol Al6Si2O13 和 4 mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3____________mol,共消耗Na2CO3 mol(得到的固体中无SiO2)。
⑶若粉煤灰中 Al6Si2O13 与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2 mol。(精确到0.01)
⑷若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2) = x,消耗Na2CO3 y mol,试确定y与x的关系式[即表示为y=f(x)]。
查看答案和解析>>
科目: 来源: 题型:
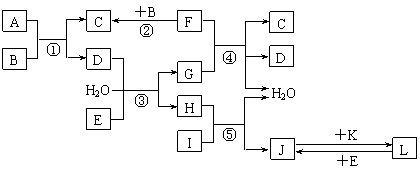 |
请回答下列问题:
(1)C的电子式为 。
(2)检验溶液L中金属阳离子的方法是 。
(3)反应③的离子方程式为 。
(4)F与G的浓溶液反应的化学方程式为 。
(5)气体A的密度为2.68g·L-1(标准状况),通过计算、推理,可确定A的分子式为 。
查看答案和解析>>
科目: 来源: 题型:
(10分)高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。
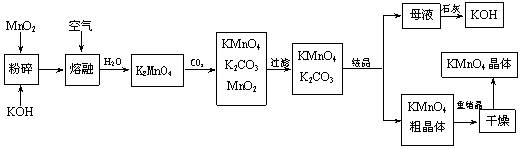 |
(1)KMnO4稀溶液是一种常用的消毒剂。其消毒机理与下列 (填序号)物质相似。
A.75%酒精 B.双氧水 C.苯酚
D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
。
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是: 。
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、 和 写化学式)。
(5)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得 mol KMnO4。
查看答案和解析>>
科目: 来源: 题型:
下列各组离子在溶液中大量共存,且加入(NH4)2Fe(SO4)2·6H2O晶体后仍能大量存在的是
A.Na+、H+、Cl—、NO3— B.K+、Ba2+、OH—、I—
C.Na+、Mg2+、Cl—、SO42— D.Cu2+、S2—、Br—、ClO—
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式与所述事实相符且正确的是
A.0.5 mol/L NaHSO4与0.5 mol/L Ba(OH)2混合至溶液呈中性:
Ba2++OH—+SO42—+H+=BaSO4↓+H2O
B.向2 mol/L Fe(NO3)2(aq)中滴加少量氢碘酸:3Fe2++NO3—+4H+=3Fe3++NO↑+2H2O
C.向20 mL 0.5 mol/L FeBr2(aq)中通入224 mL Cl2(标准状况):
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl—
D.向30 mL 0.5 mol/L NaOH(aq)中通入224 mL CO2(标准状况):
3OH—+2CO2=CO32—+HCO3—+H2O
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式表达正确的是
A.硫化钠的水解反应:S2—+2H2O ![]() H2S+2OH—
H2S+2OH—
B.铝片跟氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑
C.在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O
D.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3-
查看答案和解析>>
科目: 来源: 题型:
下列各组物质中,满足下图物质一步转化关系的选项是
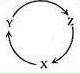
| 选项 | X | Y | Z |
| A | NO | NO2 | HNO3 |
| B | Cu | CuSO4 | Cu(OH)2 |
| C | C | CO | CO2 |
| D | Si | SiO2 | H2SiO3 |
查看答案和解析>>
科目: 来源: 题型:
下列解释不科学的是
A.“水滴石穿”主要是溶解了CO2的雨水与CaCO3长期作用生成了可溶性的Ca(HCO3)2的缘故
B.“雨后彩虹”既是一种自然现象又是光学现象,也与胶体的知识有关
C.严格地讲,“通风橱”是一种不负责任的防污染手段,因为实验产生的有害气体没有得到转化或吸收
D.长期盛放NaOH溶液的滴瓶不易打开,因为NaOH与瓶中的CO2反应使瓶内气体减少形成“负压”之故
查看答案和解析>>
科目: 来源: 题型:
(12分)甲、乙、丙、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)
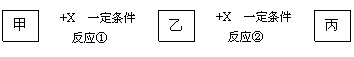
![]()
![]()
试回答下列问题:
(1)若X是强氧化性单质,则甲可能是 ▲ 。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向丙的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀。则乙的化学式为 ▲ ;丙溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示) ▲ 。
检验此丙溶液中金属元素价态的操作方法是 ▲ 。
(3)若甲、乙、丙为含有金属元素的无机化合物,X为强电解质,甲溶液与丙溶液反应生成乙;反应①的离子方程式为 ▲ ,
或 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com