
科目: 来源: 题型:
(12分) (1)下列曲线分别表示元素某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质),把与下面的元素有关性质相符合的曲线的标号填入相应括号中。
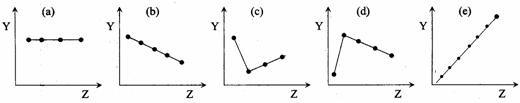 |
① ⅡA族元素的最外层电子数( ) ② ⅦA族元素氢化物的沸点( )
③ O2-、F-、Na+、Mg2+、Al3+的离子半径( ) ④第三周期元素的最高化合价( )
⑤ 第二周期元素Be、B、C、N、O的原子半径( )
(2) 比较下列性质(用“>”、“=”、“<”填空)
① 氧化性 Cl2 Br2 ② 酸性 H3PO4 H2SO4 ③ 碱性 Mg(OH)2 Al(OH)3
④ 稳定性 H2S H2O ⑤ 还原性H2S HCl
(3) 元素性质呈周期性变化的决定因素是 。
A.元素原子半径大小呈周期性变化 B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化 D.元素的最高正化合价呈周期性变化
查看答案和解析>>
科目: 来源: 题型:
(10分)(1) 已知某粒子的结构示意图为:
 试回答:
试回答:
① 当x-y=10时,该粒子为 (填“原子”、“阳离子”或“阴离子”)。
?② 当y=8时,阳离子或阴离子可能为(填离子符号): 、 、 、 。
若它们形成化合物时离子数之比为1︰2,则这些化合物的电子式为 、 。
(2) 原子序数大于4 的主族元素A和B的离子Am+和Bn-它们的核外电子排布相同,据此推断:
元素A 和B 所属周期序数之差为 ;元素A 和B 的原子序数之差为 ;元素B 和A 的最高化合价之差为 。
查看答案和解析>>
科目: 来源: 题型:
关于元素周期律和元素周期表的下列说法,正确的是
A.目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现
B.元素的性质随着原子序数的增加而呈周期性变化
C.俄国化学家道尔顿为元素周期表的建立作出了巨大贡献
D.同一主族的元素从上到下,金属性呈周期性变化
查看答案和解析>>
科目: 来源: 题型:
![]() 已知X、Y、Z为同周期三种原子序数相连的短周期元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法正确的是
已知X、Y、Z为同周期三种原子序数相连的短周期元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法正确的是
A.原子序数:Z>Y>X B.非金属活泼性:Y<X<Z?
C.原子半径:X>Y>Z? D.气态氢化物的稳定性:HX>H2Y>ZH3?
查看答案和解析>>
科目: 来源: 题型:
有A、B两种原子,A原子的M层比B原子的M层少3个电子,B原子的L层电子数恰为A原子L层电子数的2倍。A和B分别是
A.Si和Na B.B和He C.Cl和O D.C和Al
查看答案和解析>>
科目: 来源: 题型:
(9分)下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:(注:不允许用编号A~I填空)
|
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是_______,只有负价而无正价的是_______,氧化性最强的单质是_______,还原性最强的单质是_______;
(2)最高价氧化物的水化物碱性最强的是_______,酸性最强的是_______,呈两性的是_______;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的_______;
(4)在B、C、D、E、F、G、H中,原子半径最大的是_______。
查看答案和解析>>
科目: 来源: 题型:
(8分)A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族,D的最高价氧化物的水化物的酸性在同周期为最强,且B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。F元素的一种同位素的中子数为0 。
根据以上信息,回答下列问题:
(1)A和D气态氢化物中,稳定性高的是 (选填“A”或“D”)
(2)元素C在元素周期表中的位置是 。
(3)写出C的最高价氧化物的水化物分别与B、D的最高价氧化物的水化物反应的离子方程式 、
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.热稳定性:H2O >NH3> HF B. 酸性:HClO>H2SO4>H3PO4
C.碱性:KOH>NaOH>Mg(OH)2 D. 金属性:Al>Mg>Ba
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com