
科目: 来源: 题型:
若某原子在处于能量最低状态时,外围电子排布为4d15s2,则下列说法正确的是
A.该元素原子核外共有5个电子层
B.该元素原子处于能量最低状态时,原子中共有3个未成对电子
C.该元素原子的M能层共有8个电子
D.该元素原子最外层共有3个电子
查看答案和解析>>
科目: 来源: 题型:
已知锰的核电荷数为25,以下是一些同学绘制的基态锰原子核外电子的轨道表示式(即电子排布图),其中最能准确表示基态锰原子核外电子运动状态的是

A. B. C. D.
查看答案和解析>>
科目: 来源: 题型:
(12分) 工业上以氯化钾和钛白厂的副产品硫酸亚铁为原料可得到硫酸钾、过二硫酸钠和铁红颜料等产品,该方法原料的综合利用率较高。
(1)原子序数为22基态钛原子的核外电子排布式为 。
(2)TiCl4在常温下是一种无色液体,而FeCl3可用升华法提纯,则两种氯化物均属于
晶体。
(3)SO42-和 S2O82-(过二硫酸根)结构中,硫原子均位于由氧原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。下列说法正确的是 。
A. SO42-中存在σ键和π键且与PO43-离子互为等电子体
B.S2O82-中存在非极性键且有强氧化性
C.S2O82-比SO42- 稳定且两者的氧元素的化合价相同
(4)KCl与MgO的晶体结构跟NaCl的晶体结构相似,则KCl与MgO两者中熔点高的是 ,原因是 。
(5)硫与氯可形成化合物SCl2,则该分子中硫原子的杂化方式为 ,分子的空间构型为 。
(6)在一定条件下铁形成的晶体的基本结构单元如下图1和图2所示,则图1和图2的结构中铁原子的配位数之比为 。

查看答案和解析>>
科目: 来源: 题型:
下列各选项所述的两个量,前者一定大于后者的是
①Al原子和N原子的未成对电子数;②Ag+、Cu2+与NH3形成配合物时的配位数;③NaCl的晶格能与MgO的晶格能;④F元素和O元素的电负性;⑤N和O元素的第一电离能;⑥H原子和H+离子的半径
A.①④⑤ B.②④⑥ C.④⑤⑥ D.③⑤⑥
查看答案和解析>>
科目: 来源: 题型:
(6分)联氨(N2H4)是一种无色可燃的弱碱性液体,是液体大推力火箭常用的高能燃料。
⑴已知联分子中的N原子最外层满足8电子相对稳定结构,则下列说法正确的是
A.联氨(N2H4)结构与C2H4相似,存在N=N双键
B.一分子联氨中含有的电子对数目为5
C.联氨中的N原子的杂化类型为sp3杂化
D.联氨能与HCl发生化合反应生成N2H6Cl2
⑵联氨可以采用尿素[CO(NH2)2]为原料制取,方法是在高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种正盐和水,写出其反应的化学方程式 ;
⑶火箭推进器中分别装有联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。 已知:12.8 g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出256.65 kJ的热量,写出该反应的热化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
(12分)氢气、纳米技术制成的金属燃料、非金属固体燃料已应用到社会生活和高科技领域。
⑴已知短周期金属元素A和B,其单质单位质量的燃烧热大,可用作燃料。其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 899.5 | 1757.1 | 14848.7 | 21006.6 |
| B | 738 | 1451 | 7733 | 10540 |
①根据上述数据分析, B在周期表中位于 区,其最高价应为 ;
②若某同学将B原子的基态外围电子排布式写成了ns1np1,违反了 原理;
③B元素的第一电离能大于Al,原因是 ;
⑵氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由 。
②C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子相对稳定结构,则C60分子中σ键与π键的数目之比为 。
查看答案和解析>>
科目: 来源: 题型:
(15分)下表是元素周期表的一部分。
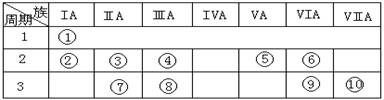
⑴下列说法正确且能说明元素⑩的非金属性比元素⑨强的是 。
A.同温同压下,元素⑩的气态氢化物溶解度大于元素⑨的气态氢化物
B.元素的最高价氧化物对应的水化物的酸性⑩强于⑨
C.元素⑨和⑩的单质与铁反应分别得到低价、高价铁的化合物
D.元素⑩的电负性大于元素⑨
⑵某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是 ,与该元素单质分子互为等电子体的二价阴离子是 。
⑶已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与盐酸反应的离子方程式:
。
⑷上述元素⑦形成的晶体对应的晶胞为下图中的___________________(填写序号)。

甲 乙 丙 丁
 ⑸元素④的含氧酸的结构式可表示为 则可判断该酸为 酸(填强或弱)
⑸元素④的含氧酸的结构式可表示为 则可判断该酸为 酸(填强或弱)
一分子该酸与水作用,只能产生1个H+,请写出该酸溶于水后溶液显酸性的离子方程式 。
⑹已知元素⑧气态氯化物的化学式为R2Cl6,结构式如下,试并标出其中的配位键
![]() Cl Cl Cl
Cl Cl Cl
Al Al
Cl Cl Cl
查看答案和解析>>
科目: 来源: 题型:
(12分)已知A、B、C、D、E、F均为周期表中前36号元素,且原子序数依次增大。A、B、C为同一周期的主族元素,B原子p能级电子总数与s能级电子总数相等。A、F原子未成对电子是同周期中最多的,且F基态原子中电子占据三种不同形状的原子轨道。D和E原子的第一至第四电离能如下表所示:
| 电离能/ kJ·mol-1 | I1 | I2 | I3 | I4 |
| D | 738 | 1451 | 7733 | 10540 |
| E | 578 | 1817 | 2745 | 11578 |
⑴A、B、C三种元素的电负性最大的是 ▲ (填写元素符号),D、E两元素中D的第一电离能较大的原因是 ▲ 。
⑵F基态原子的核外电子排布式是 ▲ ;在一定条件下,F原子的核外电子从基态跃迁到激发态产生的光谱属于 ▲ 光谱(填“吸收”或“发射”)。
⑶根据等电子原理,写出AB+的电子式: ▲ 。
⑷已知:F3+可形成配位数为6的配合物。组成为FCl3·6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3∶2∶1。则绿色配合物的化学式为 ▲ 。
A.[CrCl (H2O)5]Cl2·H2O B.[CrCl2(H2O)4]Cl·2H2O
C.[Cr(H2O)6]Cl3 D.[CrCl3(H2O)3] ·3H2O
查看答案和解析>>
科目: 来源: 题型:
(12分)目前,全世界镍(Ni)的消费量仅次于铜、铝、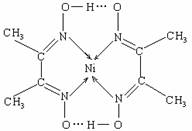 铅、锌,居有色金属第五位,镍行业发展蕴藏着巨大的潜力。
铅、锌,居有色金属第五位,镍行业发展蕴藏着巨大的潜力。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于 晶体;基态Ni原子的电子排布式为 。
(2)某配合物结构如右图所示,分子内含有的作用力
有 (填编号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
![]() (3)很多不饱和有机物在Ni催化下可与H2发生加成反应。如①CH2=CH2、②HC≡CH、③ ④HCHO等,其中碳原子采取sp2杂化的分子有 (填物质序
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。如①CH2=CH2、②HC≡CH、③ ④HCHO等,其中碳原子采取sp2杂化的分子有 (填物质序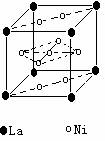 号),预测HCHO分子的立体结构为 形。
号),预测HCHO分子的立体结构为 形。
(4)氢气是新型清洁能源,镧(La)和镍的合金可做储氢材料。该合金的晶胞如右图所示,晶胞中心有一镍原子,其他镍原子都在晶胞面上。该晶体的化学式是 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选择其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
A通常显 ▲ 价,A的电负性 ▲ B的电负性(填“>”、“<”或“=”)。
(2)紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因: ▲ 。组成蛋白质的最简单的氨基酸中的碳原子杂化态是 ▲ 。
| 共价键 | C-C | C-N | C-S |
| 键能/ kJ·mol-1 | 347 | 305 | 259 |
 (3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如右图1所示),其中3种离子晶体的晶格能数据如下表:
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如右图1所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该 4种离子晶体熔点从高到低的顺序是: ▲ 。
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的
Mg2+有 ▲ 个。
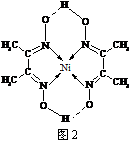 (4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 ▲ 。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 ▲ 。
(5)某配合物的分子结构如右图2所示,其分子内不含有
▲ (填序号)。
A. 离子键 B. 极性键 C. 金属键
D. 配位键 E. 氢 键 F. 非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com