
科目: 来源: 题型:
下图中a曲线表示一定条件下的可逆反应 X (g) + Y (g) ![]() 2Z (g) + W(s),正反应放热的反应过程。若使a曲线变为b曲线,可采取的措施是
2Z (g) + W(s),正反应放热的反应过程。若使a曲线变为b曲线,可采取的措施是
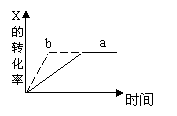 A.增大压强 B.增大X的浓度
A.增大压强 B.增大X的浓度
C.升高温度 D.加入W
查看答案和解析>>
科目: 来源: 题型:
(12分)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65KJ的热量。
(1)写出该反应的热化学方程式________________________________________________。
(2)已知H2O(l)== H2O(g);ΔH=+44 kJ·![]() ,则16g液态水气化时,放出的热量是__________________KJ。
,则16g液态水气化时,放出的热量是__________________KJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(4)已知N2(g)+ 2O2(g)== 2NO2(g);ΔH=+67.7 kJ·![]() , N2H4(g)+ O2(g)== N2(g)+ 2H2O(g);ΔH=--534 kJ·
, N2H4(g)+ O2(g)== N2(g)+ 2H2O(g);ΔH=--534 kJ·![]() 。根据盖斯定律写出肼与NO2完全反应的热化学方程式_______________________________________________。
。根据盖斯定律写出肼与NO2完全反应的热化学方程式_______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
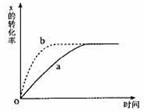 右图曲线a表示放热反应 X(g)+Y(g)
右图曲线a表示放热反应 X(g)+Y(g)![]() Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
A.升高温度
B.加大X的投入量
C.缩小容器的容积
D.增大容器的体积
查看答案和解析>>
科目: 来源: 题型:
下列对化学反应的认识正确的是
A.化学反应过程中,分子的种类和数目一定发生改变
B.如果某化学反应的DH和DS均小于0,则反应一定能自发进行
C.化学反应过程中,一定有化学键的断裂和形成
D.放热反应的反应速率,一定比吸热反应的反应速率快
查看答案和解析>>
科目: 来源: 题型:
 |
甲醇制氢气的主要途径有:
①CH3OH(g)+H2O (g)→3H2(g)+ CO2(g) △H= +49.0 kJ·mol-1
②CH3OH(g) + 1 /2O2(g) →2H2(g)+ CO2(g) △H= -192.9 kJ·mol-1
请回答下列问题:

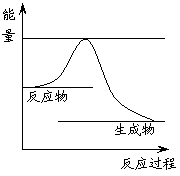 (1)反应①为 (“放”或“吸”)热反应,右图表示反应①在反应进行过程中能量(单位为kJ·mol-1)的变化示意图。试在答题纸对应的图像中用虚线表示在反应中使用催化剂后能量的变化情况。
(1)反应①为 (“放”或“吸”)热反应,右图表示反应①在反应进行过程中能量(单位为kJ·mol-1)的变化示意图。试在答题纸对应的图像中用虚线表示在反应中使用催化剂后能量的变化情况。
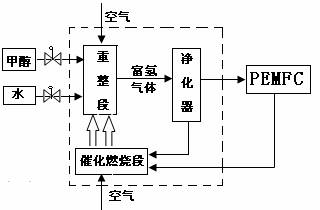
(2)催化重整段中把两种甲醇制取氢气的方法联合起来制 氢,其目的是 (写出一条即可) 。
(3)PEMFC工作时所产生的尾气(主要成份为H2)可循环应用于催化燃烧供热,则H2燃烧生成气态水时反应的热化学方程式为 。
(4)甲醇制氢质子交换膜燃料电池取代内燃机成为新一代汽车的动力,其优点有 。(填字母编号)
a.减少氮氧化物的排放 b.减少SO2的排放
c.降低对石油等化石燃料的依赖性 d.能量利用率高
查看答案和解析>>
科目: 来源: 题型:
下列有关能量转换的说法正确的是
A.煤燃烧主要是化学能转化为光能的过程
B.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.化石燃料燃烧时放出的能量均来源于太阳能
查看答案和解析>>
科目: 来源: 题型:
如下图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是
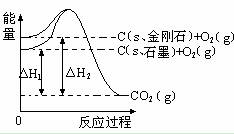
A.C(s、石墨)= C(s、金刚石) △H= +1.9 kJ•mol-1
B.石墨和金刚石的转化是物理变化
C.金刚石的稳定性强于石墨
D.1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目: 来源: 题型:
25℃和1.01×105Pa时,反应2N2O5(g)=4NO2(g)+O2(g); △H=+56.76kJ/mol,自发进行的原因是:
A.是吸热反应 B.是放热反应
C.是熵减少的反应 D.熵增大效应大于能量效应
查看答案和解析>>
科目: 来源: 题型:阅读理解
(10分)
以天然气为原料经由合成气(CO 、H2)制化学品是目前天然气转化利用的主导技术路线,主要工艺有以下几种:
(1)甲烷的部分氧化。其反应式如下:
 CH4(g) + 1/2O2 (g)=CO (g) + 2H2(g);ΔH =-35.6 kJ·mol-1。
CH4(g) + 1/2O2 (g)=CO (g) + 2H2(g);ΔH =-35.6 kJ·mol-1。
则该反应的ΔS ▲ 0(填“>”、“<”或“=”)。
有研究认为甲烷部分氧化的机理为:
① CH4(g) + 2O2 (g) =CO 2(g) + 2H2O(g);ΔH1=-890.3 kJ·mol-1
② CH4(g) + CO2 (g) = 2CO (g) + 2H2(g);ΔH2=247.3 kJ·mol-1
③ CH4(g) + H2O (g) = CO (g) + 3H2(g);ΔH3= ▲ kJ·mol-1
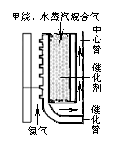
(2)甲烷水蒸汽催化重整。如右上图所示热氦气从下部流入提供能量。由甲烷和水蒸汽混合气从催化管的上部流入,从下端出来后再向上进入中心管。根据下表数据计算甲烷的转化率为 ▲ 。
| 气体 | 进口温度/℃ | 进口压强/MPa | 进口流量/g·s―1 | 出口流量/ g·s―1 |
| 甲烷 | 464 | 4.26 | 12 | 5.4 |
(3)甲烷二氧化碳催化重整。高温下,该反应速率明显降低的原因可能是 ▲ 。
(4)甲烷的部分氧化与重整耦合。以天然气为燃料的发电尾气(主要含CO2、H2O、O2 和N2)与甲烷可直接用于制合成气。下列说法错误的是 ▲ (填序号)。
A.直接利用烟气中的CO2,可以大规模地减少 CO2的排放量
B.发电尾气的出口温度较高,可以利用以节约能量
C.使用恰当的催化剂可以增大甲烷的转化率
D.因发电尾气反应中包含甲烷燃烧,可实现部分热量自供,可降低成本
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com