
科目: 来源: 题型:
(10分)我国著名化工专家侯德榜发明的侯氏制碱法的化学原理是将二氧化碳气体通入氨水的氯化钠饱和溶液中,其化学反应方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。
(1)在实验室中利用上述原理从反应所得溶液中分离出碳酸氢钠晶体,应选用下列装置中的 ,该装置使用的玻璃仪器有______、________、_______。
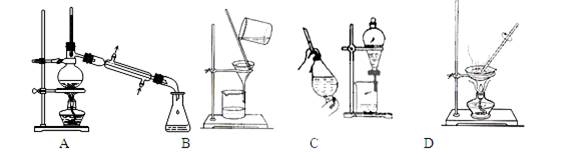
(2)实验所得碳酸氢钠晶体中,可能含有杂质离子有Cl-和NH4+,实验室鉴定Cl-所选用的试剂是 、 ,鉴定另一种杂质离子的方法是
。
(3)碳酸氢钠晶体受热分解可得到纯碱,其化学反应方程式为 。
查看答案和解析>>
科目: 来源: 题型:
(15分)现有下列10种物质:①铁片;②饱和食盐水;③液态硫酸;④乙醇;⑤干冰;⑥熔融硝酸钾;⑦碳酸钙固体;⑧铝条;⑨苛性钠;⑩石墨。
(1)用序号回答:能导电的是______________,属于电解质的是___________________,属于非电解质的是___________________。
(2)写出①与水反应的化学方程式,并用双线桥表示电子转移的方向和数目。
__________________________________________________________________
(3)写出⑧与⑨的水溶液反应的离子方程式___________________________________,该反应的氧化剂为_______________,还原产物为__________________。
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。 C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七种。
![]()
![]()
![]()
![]()
![]() 请用上述物质填空,并配平化学方程式:
请用上述物质填空,并配平化学方程式:
C+ ________+ H2SO4=== __________+ __________+
![]()
![]() Cr2(SO4)3+ H2O
Cr2(SO4)3+ H2O
若该反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为________。
查看答案和解析>>
科目: 来源: 题型:
(8分)现有A、B、C、D四种化合物的焰色反应均呈黄色。A、B、C分别和足量的盐酸反应后,均可生成D。若将固体C加热后可生成A和无色无味的气体E,若在A溶液中通入足量E,可生成C;若B与C的溶液混合可生成A。请回答下列问题:
(1)推断A、B、C、D的化学式:A_________、B___________、C_________、D__________
(2)A溶液中通入足量E反应的离子方程式为_______________________________________
(3)B溶液与C溶液反应的离子方程式为___________________________________________
查看答案和解析>>
科目: 来源: 题型:
(11分)如图所示,试推断A~Q各是什么物质?
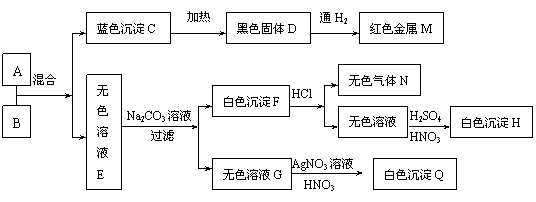 |
写出各物质的化学式:A______________;B______________;C______________;D______________;E______________;F______________;G______________;H______________;Q______________;M_____________;N_____________;
查看答案和解析>>
科目: 来源: 题型:
下列实验方法中,正确的是
A.电解MgCl2饱和溶液,可制得金属镁
B.将金属钠投入硫酸铜溶液中置换出铜
C.用氯化钙溶液鉴别碳酸氢钠与碳酸钠稀溶液
D.进行焰色反应前,应用硫酸溶液洗涤并灼烧铂丝
查看答案和解析>>
科目: 来源: 题型:
下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是
|
选项 | 甲 | 乙 | 丙 |
| A | Al2O3 | AlCl3 |
|
| B | CuO | Cu(OH)2 | CuCl2 |
| C | Fe | FeCl3 | FeCl2 |
| D | NaCl | NaHCO3 | Na2CO3 |
查看答案和解析>>
科目: 来源: 题型:
将过量的铝粉与FeO·2Fe2O3粉末配制成铝热剂w ww.ks 5u.co m,并分成两等份。一份直接放入足量的烧碱溶液中,充分反应后放出气体15.68 L(标准状况);另一份在高温下发生铝热反应,反应后的混合物与足量的盐酸反应,放出气体的体积(标准状况)可能为
A.11.20 L B.150.68 L C.22.40 L D.13.36 L
查看答案和解析>>
科目: 来源: 题型:
| 无内容 |
查看答案和解析>>
科目: 来源: 题型:
(6分)某炼
铁废渣中含有大量的CuS及少量铁的氧化物,工业上以该废渣和NaCl为原料生产CuCl2·2H2O晶体,其工艺流程中主要涉及焙烧、尾气处理、酸浸、调控溶液pH、过滤、蒸发结晶等。焙烧过程中发生的主要反应为:
CuS+2NaCl+2O2 = CuCl2+Na2SO4
请回答下列问题:
(1)焙烧时还有废气产生,其中一种是主要的大气污染物。若在实验室中以碱液吸收处理之,下列A、B、C装置中可行的是________(填字母);若选用甲装置,则烧杯中的下层液体可以是_______。
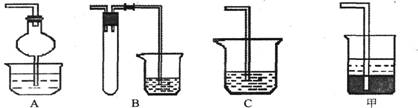
(2)调控溶液pH时采用pH试纸来测定溶液的pH,则正确的操作方法是___________________ 。
(3)若最后所得的滤液中的阴离子只有SO42-和Cl-,则检验滤液中这两种离子的实验操作为______ _ 。
查看答案和解析>>
科目: 来源: 题型:
(14分)聚合氯化铝是新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。
本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:

根据流程图回答下列问题:
⑴“煅烧”的目的是 。
⑵配制质量分数15%的盐酸需要200 mL 30%的浓盐酸(密度约为1.15 g·cm-3)和 g蒸馏水,配制用到的仪器有烧杯、玻璃棒、 。
⑶“溶解”过程中发生反应的离子方程式为 。
⑷加适量铝粉的主要作用是 。
⑸“调节溶液pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是 ;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com