
科目: 来源: 题型:
从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物;④将得到的产物熔融电解得到镁。下列说法不正确的是
A.此法的优点之一是原料来源丰富
B.①②③步骤的目的是从海水中获取MgCl2
C.提取镁的过程涉及化合、分解、置换反应
D.第④步电解时,还会产生副产品氯气
查看答案和解析>>
科目: 来源: 题型:
(8分)下图为一些常见物质的转化关系图(部分反应物与生成物未标出)。A、H为单质,其中H为气体;B、E为无色液体,F为淡黄色固体,K为红褐色固体;D的大量排放是形成酸雨的重要原因。

回答下列问题:
(l)在常温下,A和B发生的变化称为 。
(2)实验室制取F的方法是 。
(3)向C溶液中通入D,也能实现C→G的转化,则该反应的离子方程式是 。
(4)反应⑤化学方程式是
查看答案和解析>>
科目: 来源: 题型:
(8分)某同学通过查阅资料得知,铝热反应所得到的熔融物应该是铁铝合金。
(1)设计一个最简单的实验方案,证明上述所得的块状熔融物中含有金属铝。写出表示该实验原理的离子方程式: 。
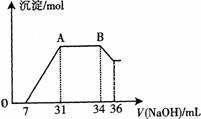 (2)某同学取一定量上述的熔融物与过量的、且很稀的硝酸充分反应,发现反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mo1·L—1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示。在AB段,有刺激性气味的气体产生。
(2)某同学取一定量上述的熔融物与过量的、且很稀的硝酸充分反应,发现反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mo1·L—1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示。在AB段,有刺激性气味的气体产生。
试回答下列问题:
①熔融物与稀硝酸充分反应后,还原产物NH4NO3的物质的量为 。
②熔融物中金属铝的物质的量为 ;金属铁的物质的量为 。
查看答案和解析>>
科目: 来源: 题型:
某AlCl3和MgCl2的混合溶液中10mL,向其中滴加amLc1mol·L—1NaOH溶液后,改成滴
加c2mol·L—1HCl,所得沉淀Y(mol)与加入的试剂总体积V(mL)
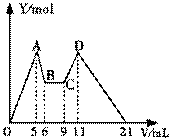 间的关系如右图所示。
间的关系如右图所示。
下列分析中正确的是:
A.上述过程中发生的离子反应共有7个
B.a=9且c1∶c2 =2∶1
C.图中D点时,溶液中有:c(Na+)=c(Cl-)
D.原混合溶液中,n(Al3+)∶n(Mg2+)=3∶2
查看答案和解析>>
科目: 来源: 题型:
(8分)已知:
![]() I H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应;
I H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应;
II 单质I2遇淀粉溶液显蓝色。
根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):

⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式: ▲ 。
⑵某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色。写出与上述变化过程相关的离子方程式: ▲ 、 ▲ 。
⑶写出Cl2将Z氧化为K2EO4的化学方程式: ▲ 。
查看答案和解析>>
科目: 来源: 题型:
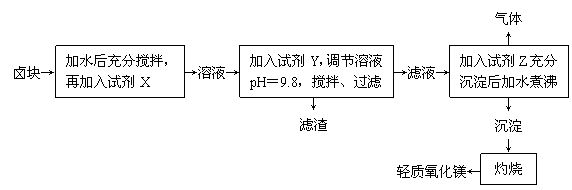 (8分)卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子。以卤块为原料制取轻质氧化镁的工艺流程如下:
(8分)卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子。以卤块为原料制取轻质氧化镁的工艺流程如下:
若要求产品中尽量不含有杂质,且生产成本较低,请根据下表中提供的资料,回答下列问题:
表1 生成氢氧化物沉淀的pH
| 物质 | 开始沉淀时的pH | 沉淀完全时的pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6☆ |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
☆ Fe2+氢氧化物呈絮状,不易从溶液中除去,故常将它氧化成Fe3+,生成Fe(OH)3沉淀除去。
表2 原料价格表
| 物质 | 价格/元·吨-1 |
| 漂液(含25%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
⑴试剂X最好是 ▲ ,加入X的作用是 ▲ 。
⑵调节pH=9.8的目的是 ▲ 。
⑶加入试剂Z后发生的离子反应方程式为 ▲ 。
⑷ 生产中产生的气体是CO2,写出产生CO2的化学方程式 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
(8分) 右图为某市售盐酸试剂瓶标签上的部分数据。
(1) 现用该浓盐酸配制200 mL 5 mol·L-1的稀盐酸。需要用量筒量取上 述浓盐酸的体积为 ▲ mL。
述浓盐酸的体积为 ▲ mL。
(2)现把1.1 g铝、铁混合物溶于200 mL 5mol/L盐酸中,反应后H+ 的浓度变为4.6mol/L(溶液体积变化忽略不计)。
该混合物中铝、铁的物质的量分别是多少?
▲
查看答案和解析>>
科目: 来源: 题型:
(7分)第29届奥运会祥云火炬的外壳材料是高强度的铝镁合金。某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金![]() 测定生成气体的体积
测定生成气体的体积
方案二:铝镁合金![]() 测定生成气体的体积
测定生成气体的体积
方案三:铝镁合金![]() 溶液
溶液![]()
![]() 称量灼烧产物的质量。
称量灼烧产物的质量。
(1)写出方案一中发生反应的离子方程式 。
(2)实验小组根据方案=设计了两个实验装置,如下圈(图中的铁架台已省略)。

你认为选择 (选填甲或乙)装置进行实验更合理,误差更小。
(3)用方案三进行实验时,除了称量灼烧产物质量外,还需称量的是 。
(4)拓展研究:在向铝镁合金溶于盐酸后的溶液中加入过量![]() 溶液时,生成沉淀的质量与加入
溶液时,生成沉淀的质量与加入![]() 溶液体积的关系可用数轴关系表示:
溶液体积的关系可用数轴关系表示:
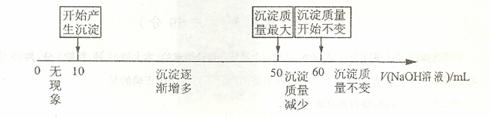
请你判断,根据上图数轴申的数据能否求出合金中镁的质量分数? (选填“能”或“不能”)
下列①②两题选一题作答。
①若不能求出合金中镁的质量分数,请说明理由 。
②若能求出合金中镁的质量分数,则镁的质量分数为 。
查看答案和解析>>
科目: 来源: 题型:
(3分) 金属是一种重要的材料,人类的生活和生产都离不开金属。目前,世界上最常见、用量最大的合金是 。铝的活动性比铁 (“强”或“弱”),但铝在空气中却比铁表现出良好的抗腐蚀性,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com