
科目: 来源: 题型:
某有机物的结构为下图所示,这种有机物不可能具有的性质是
①可以燃烧;②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应;⑥能发生水解反应
A.①④ B.只有⑥ C.只有⑤ D.④⑥
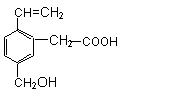
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A. 化学反应中的能量变化都表现为热量的变化
B. 需要加热才能发生的反应一定是吸热反应
C. 放热反应在常温下一定很容易发生
D. 反应是吸热还是放热必须看反应物和生成物的总能量的大小
查看答案和解析>>
科目: 来源: 题型:
关于离子键、共价键的各种叙述中,下列说法中正确的是
A.在离子化合物里,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如Cl2)中
C.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键
D.由不同元素组成的含多个原子的分子里,一定只存在极性键
查看答案和解析>>
科目: 来源: 题型:
实验室制备氨气,检验是否收集满的正确方法是
A.用手扇动收集的气体,有气味则已收集满
B.将润湿的淀粉KI试纸接近瓶口,试纸变蓝则已收集满
C.将润湿的红色石蕊试纸伸入瓶内,试纸变蓝则已收集满
D.将润湿的红色石蕊试纸接近瓶口,试纸变蓝则已收集满
查看答案和解析>>
科目: 来源: 题型:
下列化工生产原理错误的是( )
①可以电解熔融的氯化钠来制取金属钠 ②可以将钠加入氯化镁饱和溶液中制取镁 ③用电解法冶炼铝时,原料是氯化铝 ④高炉炼铁的反应是放热的,故无需加热
A.②③④ B.①③ C.①②③ D.②③
查看答案和解析>>
科目: 来源: 题型:
下列关于卤族元素由上到下性质递变的叙述,正确的是
①单质的氧化性增强 ②单质的颜色加深 ③气态氢化物的稳定性增强 ④单质的沸点升高 ⑤阴离子的还原性增强
A.①②③ B.②③④ C.②④⑤ D.①③⑤
查看答案和解析>>
科目: 来源: 题型:
关于元素周期表,下列叙述中不正确的是
A.在金属与非金属的交界处可以找到良好的半导体材料。
B.在过渡元素中可以寻找催化剂及耐高温和耐腐蚀的合金材料。
C.在元素周期表的左下角可以寻找制备新型农药材料的元素
D.目前使用的元素周期表中,最长的周期含有32种元素
查看答案和解析>>
科目: 来源: 题型:
下列比较,正确的是
A稳定性 H2S>HCl>HBr>HI B.酸性 HClO4>H2SO4>CH3COOH>H2CO3
C.粒子半径 S2-<Cl-<K+<Ca2+ D.沸点 HI>HBr>HCl>HF
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是
A. 某微粒核外电子排布的结构为
则![]() 该微粒一定是氩原子
该微粒一定是氩原子
B. r(Na+)>r(F-)
C. F-、S2-、Na+、Mg2+是与Ne原子具有相同电子层结构的离子
D. NH4+与H3O+具有相同的质子数和电子数
查看答案和解析>>
科目: 来源: 题型:
甲同学拟通过实验探究同主族元素性质的递变规律,以及影响化学反应速率的因素。其设计的实验方案如下,请你帮他填写完整,并做出评价。
实验室提供的试剂:锌块、锌粉、铁条、铁粉、铜条、NaBr溶液、NaI溶液、新制的氯水、1mol/ 盐酸、3mol/L的盐酸
(1)探究同主族元素性质的递变规律
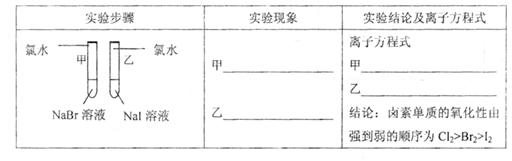
【评价】甲同学设计的实验方案的合理性是___________(填序号)
A. 非常合理 B. 部分合理 C. 完全不合理
【补充和完善】上一项若填A,则此项不用再作答,若填B或C,则完成实验还需要的试剂是___________。
(2)探究影响化学反应速率的因素
| 实验步骤 | 实验现象 | 实验依据和结论 |
|
3mL1mol/L 3mL3mol/L 盐酸 盐酸 (金属质量相同,盐酸均过量) | 均有气体生成,锌粉先消失,锌块后消失 | 因为乙试管中的反应更快,所以反应物浓度越大,反应速率越快。 |
甲同学所得实验依据和结论有明显问题,问题是__________。
(3)请你利用原电池原理,设计实验,比较铜和铁的金属活动性。画出实验装置图,标出正负极、电子流动方向,写出电极反应式。
装置图
|
|
电极反应式
____________________________
____________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com