
科目: 来源: 题型:
下列说法正确的是
A.焓变等于反应物的总能量减去生成物的总能量
B.焓变等于反应物的键能总和减去生成物的键能总和
C.断裂化学键是放热过程
D.形成新的化学键是吸热过程
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式书写正确的是
A.C(s) + O2(g) == CO2(g) ;△H= +393.5 kJ/mol
B.H2(g) + 1/2O2(g) == H2O(l);△H =-285.8 kJ/mol
C.2SO2 + O2 == 2SO3 ;△H =-196.6 kJ/mol
D.2H2(g) + O2(g) == 2H2O(l) ;△H =-571.6 kJ
查看答案和解析>>
科目: 来源: 题型:
向紫色Cr2(SO4)3溶液中,加入NaOH溶液至析出蓝灰色沉淀,此时,溶液中存在着如下平衡:Cr3+(紫色) +3OH- ![]() Cr(OH)3(蓝灰色)
Cr(OH)3(蓝灰色) ![]() CrO2- (绿色)+H+ + H2O,将上述悬浊液等分两份a和b。向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液。a、b试管中溶液颜色最终分别为
CrO2- (绿色)+H+ + H2O,将上述悬浊液等分两份a和b。向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液。a、b试管中溶液颜色最终分别为
| A | B | C | D | |
| a试管 | 紫色 | 蓝灰色 | 蓝色 | 绿色 |
| b试管 | 绿色 | 绿色 | 紫色 | 紫色 |
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.同温同压下,H2(g)+Cl2(g)==2HCl(g)在光照和点燃条件下的△H相同
B.铅蓄电池放电时的负极和充电时的阴极均发生还原反应
C.已知:H2(g) + I2(g)![]() 2HI(g);△H =-9.48 kJ/mol,若将254g I2(g)和2gH2(g)充分反应可放出9.48 kJ的热量
2HI(g);△H =-9.48 kJ/mol,若将254g I2(g)和2gH2(g)充分反应可放出9.48 kJ的热量
D.已知在101 kPa时,2 g碳燃烧生成CO放出热量为Q kJ,则碳的燃烧热为6Q kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是
A.非自发的反应即不可能进行的反应
B.自发反应即在任何条件下都能进行的反应
C.绝大多数的放热反应都能自发进行,且反应热越大,反应进行得越完全
D.吸热反应在常温、常压下不能自发进行,只有在高温下才可能自发进行。
查看答案和解析>>
科目: 来源: 题型:
pH=11的x、y两种碱溶液各5mL,分别稀释至500mL,其pH与溶液体积(V)的关系如图所示,下列结论正确的是
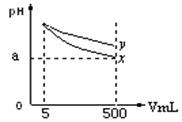
A.相同温度下,x的电离平衡常数小于y
B.若x、y是一元碱,等物质的量浓度的盐酸盐溶液,y的pH大
C.若x、y都是弱碱,则a的值一定大于9
D.完全中和x,y两溶液时,消耗同浓度稀硫酸的体积V(x)>V(y)
查看答案和解析>>
科目: 来源: 题型:
如图所示,杠杆AB两端分别持有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入较浓的硫酸铜溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中不考虑两球的浮力变化):

A.当杠杆为绝缘体时,A端高、B端低;为导体时,A端低、B端高
B.当杠杆为绝缘体时,A端低、B端高;为导体时,A端高、B端低
C.当杠杆为导体或绝缘体时,均为A端高B端低
D.当杠杆为导体或绝缘体时,均为A端低B端高
查看答案和解析>>
科目: 来源: 题型:
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是
A.镀锌层破损后即对铁制品失去保护作用
B.未通电前上述电镀装置可构成原电池,电镀过程是该原电池的充电过程
C.电镀时保持电流恒定,升高温度不改变电解反应速率
D.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系
查看答案和解析>>
科目: 来源: 题型:
已知25℃时,AgI饱和溶液中c(Ag+)为1.23×10-8mol/L,AgCl饱和溶液中c(Ag+)为1.25×10-5mol/L,若在5mL含有KCl、KI各为0.01mol/L的溶液中加入8mL0.01mol/LAgNO3溶液,则下列叙述正确的
A.混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-)
B.混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-)
C.加入AgNO3溶液时首先生成AgCl沉淀
D.混合溶液中![]() 约为1.02×10-3
约为1.02×10-3
查看答案和解析>>
科目: 来源: 题型:
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 |
A.c(HCO3-)>c(ClO-)>c(OH-)
B.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+C(OH-)
C.c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)
D.c(Na+)=c(HCO3-)+ c(CO32-) + c(H2CO3) +c(ClO-) +c(HClO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com