
科目: 来源: 题型:
已知室温下.Al(NO3)3的Ksp,或溶解度远大于Fc(OH)3。向浓度均为0.1mol·L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(NO3)3的物质的量与加入NaOH溶液的体积的关系,合理的是
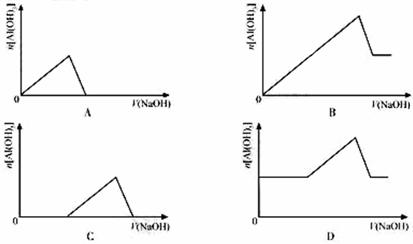
查看答案和解析>>
科目: 来源: 题型:
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时:
① HF(aq) + OH-(aq) = F-(aq) + H2O(l) △H= -67.7kJ·mol-1
② H+(aq) + OH-(aq) = H2O(l) △H= -57.3 kJ·mol-1
在20 mL0.1mol·L-1氢氟酸中加入VmL0.1 mol·L-l NaOH溶液,下列有关说法正确的是
A. 氢氟酸的电离方程式及热效应可表示为:HF(aq) ![]() F-(aq) + H+(aq) △H= +10.4kJ·mol-1
F-(aq) + H+(aq) △H= +10.4kJ·mol-1
B.当V= 20 时,溶液中:c(OH-)=c(HF)+c(H+)
C.当V=20时,溶液中:c(F-)<c(Na+)=0.1mol·L-1
D.当V>0时,溶液中一定存在:c(Na+) >c(F-) >c(OH-) >c(H+)
查看答案和解析>>
科目: 来源: 题型:
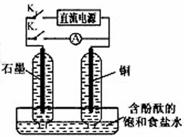
某兴趣小组设计如下微型实验装置。实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转。下列有关描述正确的是
A.断开K2,闭合K1时,总反应的离子方程式为: ![]()
B.断开K2,闭合K1时,石墨电极附近溶液变红
C.断开K1,闭合K2时,铜电极上的电极反应式为:Cl2 + 2e- = 2Cl-
D.断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目: 来源: 题型:
仅用下表提供的玻璃仪器(非玻璃仪器任选)就能实现相应实验目的的是
| 选项 | 实验目的 | 玻璃仪器 |
| A | 分离乙醇和乙酸乙酯的混合物 | 分液漏斗、烧杯 |
| B | 用PH=1的盐酸配制100mL PH=2的盐酸 | 100mL容量瓶、烧杯、玻璃棒、胶头滴管 |
| C | 用溴水、淀粉- KI溶液比较Br2与I2的氧化性强弱 | 的氧化性强弱 |
| D | 用NH4Cl固体和Ca(OH)2固体制备并收集NH3 | 酒精灯、烧杯、导管、集气瓶 |
查看答案和解析>>
科目: 来源: 题型:
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
![]()
若反应在恒容的密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时.其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
科目: 来源: 题型:
下列离子或分子在溶液中能大量共存,通入CO2后仍能大量共存的一组是
A.K+ 、Ca2+ 、Cl- 、NO3- B.K+ 、Na+、Br-、SiO32-
C. H+ 、Fe2+ 、SO42- 、Cl2 D.![]()
查看答案和解析>>
科目: 来源: 题型:
科学家最近研究出一种环保、安全的储氢方法,其原理可表示为为:
![]()
A.储氢、释氢过程均无能量变化 B.NaHCO3、HCOONa均含有离子键和共价键
C.储氢过程中,NaHCO3被氧化 D.释氢过程中,每消耗0.1molH2O放出2.24L的H2
查看答案和解析>>
科目: 来源: 题型:
元素X、Y、Z、M、Q均为短周期主族元素,且原子序数依次增大。已知元素Y最高价氧化物对应水化物与它的氢化物反应能生成一种盐;Z原子最外层电子数与核外电子总数之比为3:4;M可与Z形成阴、阳离子个数比为1:2的两种化合物,Q原子的最外层电子数与次外电子数之比为3:4,YX3常温下为气体。
(1)化合物A、B由X、Z、M、Q四种元素中的三种组成的强电解质,且A属于碱,B属于盐,组成元素的原子数目之比均为1:1:1,则化合物A的化学式为 ,B的化学式是 。
(2)Se是人体必备的微量元素,与Q同一主族。该族二至五周期元素单质分别与H2反应生成1mol 气态氢化物的反应热如下,表示生成1 mol哂化氢反应热(△H)的是 (填字母代号)。
A.+99.7kJ·mol-1 B.+29.7 kJ·mol-1
C.-20.6 kJ·mol-1 D.-241.8 kJ·mol-1
(3)X与Z、X与Q均可形成18电子分子甲和乙,写出甲、乙两种分子在水溶液中反
应生成Q单质的化学方程式 。X和Y也可形成18电子分子丙,它通常是一种液态火箭燃料。25℃、常压下,3.2g丙在氧气中完全燃烧放出热量为62.4kJ,请写出丙完全燃烧的热化学反应方程式 。
(4)X、Y两种元素形成的离子化合物的电子式为 。
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分,回答下列有关问题:
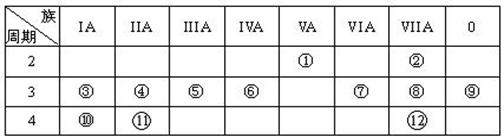
⑴.写出下列元素符号:① ⑥ ⑦
⑵.在①~⑫元素中,金属性最强的元素是 ,非金属性最强的元素是 ,最不活泼的元素是 。(均填元素符号)
⑶.元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.常温下⑦的单质和⑧的单质状态不同 b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
⑷.第三周期中原子半径最大的元素是 (填序号),跟它同周期原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。
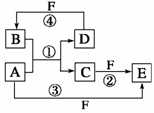
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为________,反应④的化学方程式为______________________________。
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行。反应②也在水溶液中进行,其离子方程式是__________________________________,
用电子式表示化合物B的形成过程:_______________________________。
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素
同周期,则反应①的化学方程式为___________________________________。
(3)同族非金属元素之间相互置换的一般是第ⅣA、第ⅥA、第 ⅦA。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com