
科目: 来源: 题型:
碳酸氢铵是一种重要的铵盐。实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱。
完成下列填空:
41.二氧化碳通入氨水的过程中,先有__晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体。
42.含0.800 mol NH3的水溶液质量为54.0 g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为____%。
43.粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:
①粗盐溶解;②加入试剂至沉淀完全,煮沸;③__;④加入盐酸调pH;⑤加入__;⑥过滤;⑦灼烧,冷却,称重。
44.上述步骤②中所加入的试剂为__、__。
45.上述步骤④中加盐酸调pH的目的是__。
46.为探究NH4HCO3和NaOH的反应,设计实验方案如下:
含0.1 mol NH4HCO3的溶液中加入0.1 mol NaOH,反应完全后,滴加氯化钙稀溶液。
若有沉淀,则NH4HCO3与NaOH的反应可能为_____(写离子方程式);
若无沉淀,则NH4HCO3与NaOH的反应可能为______(写离子方程式)。
该实验方案有无不妥之处?若有,提出修正意见。
查看答案和解析>>
科目: 来源: 题型:
碱式碳酸铜【Cu2(OH)2CO3】是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
步骤一:废铜屑制硝酸铜
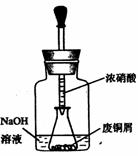
如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
 完成下列填空:
完成下列填空:
35.写出浓硝酸与铜反应的离子方程式。
36.上图装置中NaOH溶液的作用是__。反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有____(填写化学式)。
37.步骤二中,水浴加热所需仪器有____、__(加热、夹持仪器、石棉网除外);洗涤的目的是____。
38.步骤二的滤液中可能含有CO32-,写出检验CO32-的方法。
39.影响产品产量的主要因素有____。
40.若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是____。
查看答案和解析>>
科目: 来源: 题型:
用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g)+Q(Q>0)
Si3N4(s)+12HCl(g)+Q(Q>0)
完成下列填空:
31.在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增加了2.80 g,则H2的平均反应速率___ mol/(L·min);该反应的平衡常数表达式K=_____
32.上述反应达到平衡后,下列说法正确的是_。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4物质的量平衡向左移动
d.其他条件不变,增大HCl物质的量平衡向左移动
33.一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是__。
a.3v逆(N2)=v正(H2) b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变 d.c(N2):c(H2):c(HCl)=1:3:6
34.若平衡时H2和HCl的物质的量之比为![]() ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___![]() (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
完成下列填空:
27.Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式________。
28.已知:Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O→Se+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是______。
29.回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3→Se+I2+KNO3+H2O
②I2+2Na2S2O3→Na2S4O6+2NaI
配平方程式①,标出电子转移的方向和数目。
30.实验中,准确称量SeO2样品0.1500g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为___。
查看答案和解析>>
科目: 来源: 题型:
2009年《自然》杂志报道了我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。
完成下列填空:
23.10Be和9Be_______。
a.是同一种原子 b.具有相同的中子数
c.具有相同的化学性质 d.具有恒定的丰度
Be所在的周期中,最外层有2个未成对电子的元素相互组成的化合物属于_____晶体。
24.Al和Be具有相似的化学性质,写出BeCl2水解反应的化学方程式_____。
25.研究表明26Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是____。
a.比较这两种元素的单质的硬度和熔点
b.在氯化铝和氯化镁的溶液中分别滴加过量的氢氧化钠溶液
c.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液
d.将空气中放置已久的这两种元素的单质分别和热水作用
26.目前还有一种测量方法叫“钾氩测年法”。写出和Ar核外电子排布相同的阴离子的半径由大到小的顺序______(用化学符号表示);其中一种离子与钾相邻元素的离子所形成的化合物可用做干燥剂,此化合物的电子式是_______。
查看答案和解析>>
科目: 来源: 题型:
PbO2是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1 mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3:2,则剩余固体的组成及物质的量比是
A.1:1混合的Pb3O4、PbO B.1:2混合的PbO2、Pb3O4
C.1:4:1混合的PbO2、Pb3O4、PbO D.1:1:4混合的PbO2、Pb3O4、PbO
查看答案和解析>>
科目: 来源: 题型:
常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判断一定错误的是
A.若c(OH-)>c(H+),a=b B.若c(K+)>c(CH3COO-),a>b
C.若c(OH-)=c(H+),a>b D.若c(K+)<c(CH3COO-),a<b
查看答案和解析>>
科目: 来源: 题型:
火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2
下列说法正确的是
A.SO2既是氧化产物又是还原产物
B.CuFeS2仅作还原剂,硫元素被氧化
C.每生成1 molCu2S,有4mol硫被氧化
D.每转移1.2 mol电子,有0.2 mol硫被氧化
查看答案和解析>>
科目: 来源: 题型:
含有下列各组离子的溶液中,通入过量SO2气体后仍能大量共存的是
A.H+、Ca2+、Fe3+、N03- B.Ba2+、Cl-、Al3+、H+
C.Na+、NH4+、I-、HS- D.Na+、Ca2+、K+、Cl-
查看答案和解析>>
科目: 来源: 题型:
为探究锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是
A.加入NH4HSO4固体,v(H2)不变 B.加入少量水,v(H2)减小
C.加入CH3COONa固体,v(H2)减小 D.滴加少量CuSO4溶液,v(H2)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com