
科目: 来源: 题型:
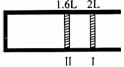
恒温、恒压下,将1mol O2和2mol SO2气体充入一体积可变的容器中(状态Ⅰ),发生反应2SO2+O2![]() 2SO3,状态Ⅱ时达平衡,则O2的转化率为( )
2SO3,状态Ⅱ时达平衡,则O2的转化率为( )
A.40% B.60% C.80% D.90%
查看答案和解析>>
科目: 来源: 题型:
2008年10月8日,瑞典皇家科学院宣布美籍华裔科学家钱永健获得2008年度诺贝尔化学奖.少年时代,他就对化学产生了浓厚的兴趣。16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获具有“少年诺贝尔奖”之称的著名奖项。下列说法正确的是( )
A.金属腐蚀就是金属失去电子被还原的过程
B.将水库中的水闸(钢板)连接一块锌块,可防止水闸被腐蚀
C.由原电池原理知所有的合金都比纯金属更易被腐蚀
D.铜板上的铁铆钉处在潮湿的空气中发生:Fe-3e-===Fe3+,从而形成铁锈,但此过程铜不被腐蚀
查看答案和解析>>
科目: 来源: 题型:
体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2![]() 2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( )
2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( )
A.等于p% B.大于p% C.小于p% D.无法判断
查看答案和解析>>
科目: 来源: 题型:
将2 mol A和1 mol B充入一个密闭容器中,在一定条件下发生:2A(g)+B(g)![]() xC(g)达到平衡,测得C的物质的量分数为c%;若开始充入容器中的是0.6 mol A,0.3 mol B和1.4 mol C, 达平衡时C的物质的量分数仍为c%,则x的值可能为 ( )
xC(g)达到平衡,测得C的物质的量分数为c%;若开始充入容器中的是0.6 mol A,0.3 mol B和1.4 mol C, 达平衡时C的物质的量分数仍为c%,则x的值可能为 ( )
A、2 B、3 C、4 D、5
查看答案和解析>>
科目: 来源: 题型:
下列关于实验现象的描述不正确的是 ( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片作负极,铁片作正极,稀硫酸为电解质溶液一段时间后,溶液PH增大
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓海轮腐蚀
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是 ( )
A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.将甲、乙作电极组成原电池时,甲是正极
查看答案和解析>>
科目: 来源: 题型:
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(![]() )中而形成的,电池总反应方程式为:
)中而形成的,电池总反应方程式为:
8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是 ( )
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4∶1
查看答案和解析>>
科目: 来源: 题型:
某化学教师为“氯气与金属钠反应”设计了如图装置与操作以替代相关的教材上的实验。实验操作:先给钠预热,当钠熔成圆球时,撤火、通入氯气,即可见钠着火燃烧,并产生大量白烟。以下叙述错误的是( )
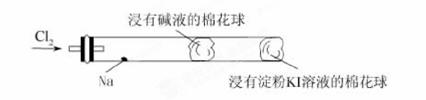
A.钠着火燃烧产生苍白色火焰
B.反应生成的大量白烟是氯化钠晶体
C.管中部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
D.管右端棉球外颜色变化可判断氯气是否被碱液完全吸收
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com