
科目: 来源: 题型:
(6分)(1)、将CO、O2 2种气体分别盛放在2个容器中,并保持2个容器内气体的温度和密度均相等,这2种气体对容器壁所施压强的大小关系是 。
(2)、同温、同压下某瓶充满O2时重116克,充满CO2重122克,充满某气体时重114克。则某气体的相对分子质量为 。
(3)、A物质按下式分解:2A=B↑+2C↑+2D↑,测得生成的混合气体在相同条件下的密度是H2密度的m倍,则A的摩尔质量为 。
查看答案和解析>>
科目: 来源: 题型:
(11分)用18mol/L浓硫酸配制480ml1.0mol/L稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积②量取一定体积的浓硫酸③稀释④转移、洗涤⑤定容、摇匀
回答下列问题
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 。
A、10ml B、25ml C、50ml D、100ml
(2)实验需要的仪器除容量瓶、烧杯、量筒外,还需要 。
(3)第③步实验的操作是
。
(4)下列情况对所配制的稀硫酸浓度有何影响(用偏大、偏小、无影响填写)
A、所用的浓硫酸长时间放置在密封不好的容器中 。
B、容量瓶用蒸馏水洗涤后残留有少量的水 。
C、未冷却至室温即转移并定容
D、定容时俯视溶液的凹液面
查看答案和解析>>
科目: 来源: 题型:
(11分)使用启普发生器制取气体,具有随时可控制反应进行和停止的优点。某化学兴趣小组制作了如图所示的装置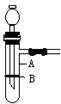 ,代替启普发生器。
,代替启普发生器。
(1)图中A仪器的名称是 ,缺少的仪器是 ,
(2)制作B使用的是( )
A、铁片 B、铝箔 C、纸片 D、塑料片
(3)在该装置中用下列反应制气体,反应原理可行,且可能达到上述优点的是( )
A、Na2CO3·10H2O+HCl→CO2↑ B、Cu+H2SO4→H2↑ C、CaCO3+HNO3→CO2↑
(4)若用该装置进行锌粒与稀硫酸反应制取氢气的实验;对装置作气密性检查的方法是 ,
(5)向装置中加入锌粒的方法是 。
(6)当需反应停止时的操作和发生的现象是 。
查看答案和解析>>
科目: 来源: 题型:
(8分)右图为实验室某浓盐酸试剂瓶标签上的有关数据,根据有关数据回答下列问题:
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/m3 质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为 mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少 而变化的是 。
A、溶液中HCl的质量 B、溶液的p H
C、溶液中H+的数目 D、溶液的密度
(3)欲配制上述浓盐酸,需要在1L水中通入标态下 L
HCl气体(保留1位小数)
(4)现有1L1mol/L的稀盐酸,欲使其浓度增大1倍,采取的措施合理的是 。
A、通入标况下HCl气体22.4L B、将溶液加热浓缩至0.5L
C、加入5mol/L的盐酸0.6L,再稀释至2L。 D、加入1L 3mol/L的盐酸混合均匀。
查看答案和解析>>
科目: 来源: 题型:
(8分)计算以下两小题时,除必须应用所有给出的数据外,还各缺少一个数据,指出该数据的名称(分别以a和b表示),并列出计算式。
(1)在温度为t℃和压强pPa的情况下,19.5g A与11.0g B恰好完全反应,生成固体C和3.00L的D气体,计算生成的C的质量(m)。缺少的数据是 ,
计算式为m= 。
(2)0.48g金属镁与10mL盐酸反应,计算生成的H2在标准状况下的体积[V(H2)]。缺少的数据是 ,计算式为
查看答案和解析>>
科目: 来源: 题型:
氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括 ( )
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A.①② B.①③ C.③④ D.②④
查看答案和解析>>
科目: 来源: 题型:
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是 ( )
A.CH3OH(l)+3/2O2(g) → CO2(g)+2H2O(l) △H=+725.8 kJ/mol
B.2CH3OH(l)+3O2(g)→ 2CO2(g)+4H2O(l) △H=-1452 kJ/mol
C.2CH3OH(l)+3O2(g)→ 2CO2(g)+4H2O(l) △H=-725.8 kJ/mol
D.2CH3OH(l)+3O2(g)→ 2CO2(g)+4H2O(l) △H=+1452 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
下列各组热化学方程式中,化学反应的△H前者大于后者的是 ( )
①C(s)+O2(g)===CO2(g);△H1 C(s)+1/2O2(g)===CO(g);△H2
②S(s)+O2(g)===SO2(g);△H3 S(g)+O2(g)===SO2(g);△H4
③H2(g)+1/2O2(g)===H2O(l);△H5 2H2(g)+O2(g)===2H2O(l);△H6
④CaCO3(s)===CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)===Ca(OH)2(s);△H8
A.① B.④ C.②③④ D.①②③
查看答案和解析>>
科目: 来源: 题型:
把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上有大量气泡产生,则四种金属的活动性顺序由强到弱为 ( )
A.a>b>c>d B.a>c>d>b C.c>a>b>d D.b>d>c>a?
查看答案和解析>>
科目: 来源: 题型:
在2A+B 3C+4D反应中,表示该反应速率最快的是 ( )
A.v(A)=0.5 mol·L-1·s-1 B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1 D.v(D)=1 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com