
科目: 来源: 题型:
某溶液中含有NH、SO、SiO、Br-、CO、Na+,向该溶液中通入过量的Cl2,下列判断正确的是 ( )
①反应前后,溶液中离子浓度基本保持不变的有NH、Na+
②有胶状沉淀生成
③有气体产生
④溶液颜色发生变化
⑤共发生了2个氧化还原反应
A.①②③④ B.②③④ C.①③⑤ D.②④⑤
查看答案和解析>>
科目: 来源: 题型:
若NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.1 molSiO2晶体中含有NASiO2个分子
B.7.8 g Na2O2中含有的离子总数目为0.4NA
C.标准状况下2.24L苯含有的碳原子数目为0.6NA
D.12.8g Cu与足量HNO3反应生成NO和NO2,转移电子数目为0.4NA'
查看答案和解析>>
科目: 来源: 题型:
CH4催化还原NOx可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g); ΔH=-574 kJ/mol
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g); ΔH=-1160kJ/mol
下列说法不正确的是 ( )
A.反应①②均为放热反应
B.反应①②转移的电子数相同
C.由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ/mol,a<574
D.若用标准状况下4.48 LCH4通过上述反应还原NO2至N2,放出的热量为173.4 kJ
查看答案和解析>>
科目: 来源: 题型:
(15分)有A、B、C、D、E五种短周期元素,其元素特征信息如下表
| 编号 | 元素特征信息 |
| A | 其单质是密度最小的物质。 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一。 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物。 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(1)E元素的名称是 。
(2)A、B、C形成的化合物的电子式为 ,该化合物中含有的化学键是 。
(3)B、C、D的简单离子半径由大到小的顺序是(用离子符号表示) 。
(4)①E单质与A、B、C形成的化合物反应的化学方程式为
;
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式为
;
③B、C元素形成的两种化合物与A2B反应的两个化学方程式:
、
查看答案和解析>>
科目: 来源: 题型:
(18分)食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量Ca2+、Mg2+、Fe3+、SO42-等杂质离子,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
步骤1:取一定量的粗盐,置于烧杯中,加入足量的水,配成粗盐水;
步骤2:向粗盐水中加入除杂试剂,然后进行过滤,滤去不溶物,再向滤液中加入盐酸调
节盐水的pH;
步骤3:将得到的溶液蒸发浓缩、冷却、结晶、过滤、烘干即得精盐;
请回答以下问题:
①上述实验中的过滤操作需要烧杯、____________、____________等玻璃仪器.
②步骤2中常用Na2CO3、NaOH、BaCl2作为除杂试剂,则加入除杂试剂的顺序为:
、 、 NaOH。
③步骤2中,判断加入BaCl2已过量的方法是
________________________。
(2)为检验精盐纯度,需配制100 mL 0.5mol/L(精盐)溶液,右图是该
同学转移溶液的示意图,图中的错误是
________________________________________________。
若在定容时仰视,则所配溶液的浓度_______0.5mol/L(填>或<)。
(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,
则相同条件下收集的Cl2 (填>、=或<)
2L,原因
(4)某学习小组设计了如下图实验,将氯气依次通过下列装
置以验证氯气的性质:
①通入氯气后,A中的现象是 ,整套实验装置存在的明显缺
陷是 。
②C装置中发生反应的离子方程式为 。
③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤):
查看答案和解析>>
科目: 来源: 题型:
(15分)某强酸性溶液X中含有Ba2+、A l3+、NH4+、Fe2+、Fe3+、CO32—、SO32—、SO42—、Cl—、NO3—中的一种或几种,取该溶液进行连续实验,实验过程如下:
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还一定含有的离子是____________________,不能确定的阳离子是___________,若要用实验证明该离子一定不存在,其最可靠的化学方法是________________________________________________________。
(2)沉淀G的化学式为_____________。
(3)写出下列反应的离子方程式:
①中生成气体A:_______________________________________。
②生成沉淀I:_______________________________________________。
(4)假设测定A、F、I均为0.01mol,10mL X溶液中n(H+)=0.04mol,且不能确定含有的离子只有一种。当X溶液中不能确定离子是_________,沉淀C物质的量___________。
查看答案和解析>>
科目: 来源: 题型:
(12分)A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如下所示:
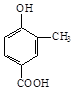
![]()

A B C D
回答下列问题:
(1)化合物C的分子式为 ,C中的含氧官能团名称是 。
(2)1molB最多能与 molH2发生反应,B与新制Cu(OH)2反应的产物的结构简式
为 。
(3)D发生聚合反应的产物的结构简式为 。
(4)A能与乙醇发生反应生成一种有特殊香味的物质,请写出该反应的方程式:
(5)关于上述四种物质的说法中正确的是
A.都能与Na反应放出H2
B.C、D均能使溴的四氯化碳溶液褪色
C.A和C均能与NaHCO3溶液反应放出CO2
D.1molC最多能与4molBr2发生反应
查看答案和解析>>
科目: 来源: 题型:
化学与科技、生活、环境密切相关,下列说法正确的是①光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅
②棉、麻、丝、毛及合成纤维完全燃烧都是只生成CO2和H2O
③为防止电池中的重金属污染土壤和水体,应将废电池深埋
④不能将铁制自来水管与铜制水龙头连接
⑤自来水厂在处理水时常加入硫酸铁和氯气,能同时达到消毒杀菌和除去水中悬浮杂质的作用
⑥pH在5.6~7.0之间的降水可通常称为酸雨
⑦汽车尾气中氮氧化物、一氧化碳、碳氢化合物和颗粒物等,严重污染大气
⑧常见的银纪念币制作时一般为铜芯镀银,铜芯应做阳极
A.①②④⑦⑧ B.②④⑦⑧ C.④⑤⑦ D.②③⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
NA表示阿伏加德罗常数,下列有关叙述正确的是
①1mol苯乙烯中含有的碳碳双键数为4NA
②6.2g氧化钠和7.8g过氧化钠的混合物中含有的离子总数为0.6NA
③3.4gNH3中含N—H键数目为0.2NA
④常温下1L0.5mol/L NH4Cl溶液与2L0.25mol/L NH4Cl溶液所含NH4+的物质的量相同
⑤在标准状况下,22.4L 甲烷与18g水所含有的电子数均为10NA
⑥等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1
⑦56 g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA
⑧1mol固体NaHSO4含有的阴阳离子总数为2NA
A.①④⑦ B.②⑤⑧ C.②③④⑥ D.①②④⑤⑦
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式不正确的是
①用FeCl3溶液腐蚀铜线路板: Cu + Fe3+ = Cu2+ +Fe2+
②将含等物质的量的NaHCO3和Ba(OH)2溶液混合:
HCO3-+Ba2++OH-== BaCO3↓+H2O
③NH4HSO3溶液与足量NaOH溶液混合加热:
NH4+ +HSO3- + 2OH-NH3↑+ SO32-+2H2O
④将氯气溶于水制备次氯酸: Cl2+H2O= 2H+ + Cl- + ClO-
⑤食醋除水垢中的碳酸钙: CaCO3 + 2H+ = Ca2++ H2O +CO2↑
⑥苯酚钠溶液中通入少量的CO2气体: C6H5O- + CO2 +H2O→C6H5OH + HCO3-
A.①②④⑥ B.③④⑤ C.①④⑤ D.③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com