
科目: 来源: 题型:
某溶液中含有![]() 、
、![]() 、
、![]() ,现用
,现用![]() 溶液、盐酸和
溶液、盐酸和![]() 溶液将这三种离子逐一沉淀分离,其流程如下图所示。
溶液将这三种离子逐一沉淀分离,其流程如下图所示。
下列说法正确的是( )
A.试剂A为![]() 溶液
溶液
B.沉淀3的化学式可能是![]()
C.生成沉淀1的离子方程式为:![]() +2
+2![]() =
=![]() ↓
↓
D.生成沉淀2的离子方程式为:![]() +
+![]() =
=![]() ↓
↓
查看答案和解析>>
科目: 来源: 题型:
下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
A.只有①④ B. 只有③ C.只有②③ D. 只有①③④
查看答案和解析>>
科目: 来源: 题型:
加热一定量的碳酸氢钠固体至200℃,将产生的全部气体用足量的过氧化钠粉末完全吸收得到固体M,取一定量的固体M与V mL C mol·L—1盐酸恰好完全反应得到中性溶液和混合气体X,则混合气体X的物质的量为(不考虑溶液中溶解气体) ( )
A.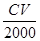 mol B.
mol B.![]() mol C.
mol C.![]() mol<n(X)<
mol<n(X)<![]() mol D.无法计算
mol D.无法计算
查看答案和解析>>
科目: 来源: 题型:
某溶液中除H+、OH—外,还含有大量的Mg2+、Fe3+、Cl—,且这三种离子的物质的量浓度之比为1:1:6。下列有关该溶液的判断正确的是( )
A. 向该溶液中加入KI溶液后,原有的五种离子的物质的量不变
B. 向该溶液中滴加稀NaOH溶液,立即出现白色沉淀
C. 若溶液中c(Cl—) = 0.6 mol/L,则该溶液的pH为1
D. 向该溶液中加入过量铁粉,只发生置换反应
查看答案和解析>>
科目: 来源: 题型:
向含Fe(NO3)3、Cu(NO3)2、HNO3的稀溶液中逐渐加入铁粉,![]() 的变化如图所示。下列离子方程式错误的是( )
的变化如图所示。下列离子方程式错误的是( )
A. 0~1 : Fe+ NO3—+4H+=Fe3++ NO↑+2H2O B. 1~2 : Fe+2Fe3+=3Fe2+
C. 2~3 :Fe+Cu2+=Fe2++Cu D. 0~3 : 3Fe+2Fe3++2Cu2+=5Fe2++2Cu
查看答案和解析>>
科目: 来源: 题型:
9.7 g Cu和Zn的合金与足量的稀HNO3反应,还原产物只有NO气体,其体积在标准状况下为2.24 L,将溶液稀释为1 L,测得溶液的pH=1,此时溶液中NO3-的浓度为( )
A. 0.3 mol·L—1 B. 0.4 mol·L—1 C. 0.5 mol·L—1 D. 0.6 mol·L—1
查看答案和解析>>
科目: 来源: 题型:
(12分)下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。
(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为_________(填代号)。能验证CO氧化产物的现象是____________。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应_________,活塞b应_________,需要加热的仪器装置有_________(填代号),m中反应的化学方程式为____________。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有:____________。
②实验中观察到E内有红棕色气体出现,证明氨气具有_________性。
查看答案和解析>>
科目: 来源: 题型:
(12分)工业上将纯净干燥的氯气通入到物质的量浓度为0.375mol/L的NaOH溶液中得到漂水。某同学在实验室利用下述实验装置探究Cl2性质并模拟制备漂水。
(1)配制470mL物质的量浓度为0.375 mol/L的NaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 。
(2)浓硫酸的作用是______________________。
(3)装置E中发生反应的离子方程式为______________________________________。
(4)装置B中饱和NaCl溶液可用于除去Cl2中的HCl气体,已知氯气与水的反应是一个可逆反应,请简述用饱和NaCl溶液除去Cl2中HCl气体的原理(用离子方程式表示,并配必要的文字说明)
。
(5)实验时装置D中湿润的红色纸条褪色,干燥部分没有褪色,放置一段时间后,纸条全部褪色。该同学认为Cl2的密度比空气大,可能是试管下部Cl2的浓度大于试管上部Cl2的浓度所导致的。请判断该解释是否合理,并分析产生上述实验现象的原因_________________
_________________________________________。
(6)如果制得氯元素含量为10%的漂水溶液35.5g,那么其中含NaClO的物质的量为____mol。
查看答案和解析>>
科目: 来源: 题型:
(10分) 以黄铜矿(主要成份为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下:
已知:①4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O;
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表:
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 6.7 | 3.7 | 9.6 |
(1)试剂a是___________,试剂b是_____________。
(2)操作X应为蒸发浓缩、________________、________________。
(3)反应Ⅱ中加CuO调pH为3.7~4的目的是
。
(4)反应Ⅴ的离子方程式为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com