
科目: 来源: 题型:
右图是一种可充电的锂离子电池充放电的工作示意图。
放电时该电池的电极反应式为:
负极:LixC6-xe-=C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)
正极:Li1-xMnO2+xLi++x e-=LiMnO2(LiMnO2表示含锂原子的二氧化锰)
下列有关说法正确的是( )
A.该电池的反应式为Li1-xMnO2+LixC6LiMnO2+C6
B.K与M相接时,A是阳极,发生氧化反应
C.K与N相接时,Li+由A极区迁移到B极区
D.在整个充、放电过程中至少存在3种形式的能量转化
查看答案和解析>>
科目: 来源: 题型:
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列分析中正确的是( )
A.白色沉淀是CuI2,棕色溶液含有I2
B.滴加KI溶液时,转移1mole-时生成2mol白色沉淀
C.上述实验条件下,物质的氧化性:Cu2+>I2>SO2
D.通入SO2时,SO2与I2反应,I2作还原剂
查看答案和解析>>
科目: 来源: 题型:
下列有关溶液中粒子浓度的关系式中,正确的是( )
A.pH相同的①CH3COONa、②NaHCO3、③C6H5ONa三份溶液中的c(Na+):③>②>①
B.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中: c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.右图中pH=7时:c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
D.右图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)

查看答案和解析>>
科目: 来源: 题型:
在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3 X(g)+Y(g)![]() 2 Z(g) ΔH<0
2 Z(g) ΔH<0
保持温度不变,测得平衡时的有关数据如下:
|
| 恒容容器甲 | 恒压容器乙 |
| X的物质的量(mol) | n1 | n2 |
| Z的体积分数 | φ1 | φ2 |
下列说法正确的是( )
A.平衡时容器乙的容积一定比反应前小
B.平衡时容器甲的压强一定比反应前小
C.n2>n1
D.φ2>φ1
查看答案和解析>>
科目: 来源: 题型:
(10分)活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
已知:几种离子生成氢氧化物沉淀时的pH如下表:
| 待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请问答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是 ▲ ,该步骤需控制溶液pH的范围是 ▲ 。
(2)A溶液中主要含有的溶质是 ▲ 。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应△H>0,该反应能自发进行的原因是:△S ▲ (选填“=”、“>”、“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为 ▲ mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。
查看答案和解析>>
科目: 来源: 题型:
(14分)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:
(1)在农业生产中,滤液1可用作 ▲ 。
(2)上述氧化过程中,发生反应的离子方程式是: ▲ ,控制反应温度30℃以下的原因是: ▲ 。
(3)结晶过程中加入浓KOH溶液的作用是: ▲ 。
(4)某温度下,将Cl2通入KOH溶液中,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ▲ 。
(5)实验测得铁盐溶液的质量分数、反应时间与K2FeO4产率的实验数据分别如图1、图2所示。为了获取更多的高铁酸钾,铁盐的质量分数应控制在 ▲ 附近、反应时间应控制在 ▲ 。


查看答案和解析>>
科目: 来源: 题型:
(14分)工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下:
Ⅰ、碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
Ⅱ、25℃时有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe (OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
回答下列问题:
(1)加入NaOH溶液时发生的离子方程式为:
▲ 。
25℃时,向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的
pH=8时,c(Mg2+):c(Fe3+)= ▲ 。
(2)“趁热过滤”时的温度应控制在 ▲ 。
(3)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。
请你分析实际工业生产中是否可行 ▲ ,并说明理由:
▲ 。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10 H2O(g) △H=+ 532.36kJ·mol-1
Na2CO3·10H2O (s)=Na2CO3·H2O(s)+9 H2O(g) △H=+ 473.63kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
(15分)某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如图所示),大大地提高了资源利用率,减少了环境污染。
请填写下列空白:
(1)写出钛铁矿经氯化得到四氯化钛的化学方程式: ▲ 。
(2)由CO和H2合成甲醇的方程式是:CO(g)+2H2(g) CH3OH(g)。
①已知该反应在300℃时的化学平衡常数为0.27,该温度下将2 mol CO、3 mol H2和2 mol CH3OH充入容积为2 L的密闭容器中,此时反应将 ▲ (填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
②若不考虑生产过程中物质的任何损失,该产业链中每合成19.2 t甲醇,至少需额外补充H2 ▲ t。
(3)用甲醇—空气碱性(KOH)燃料电池作电源电解精炼粗铜(右图),

在接通电路一段时间后纯Cu质量增加3.2 g。
①请写出燃料电池中的负极反应式: ▲ 。
②燃料电池正极消耗空气的体积是 ▲ (标准状况,
空气中O2体积分数以20%计算)。
查看答案和解析>>
科目: 来源: 题型:
(15分)以铬铁矿[主要成份为Fe(CrO2)2,含有Al2O3、Fe2O3、SiO2等杂质]为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下:


(1)煅烧过程中,铬铁矿中的Al2O3与纯碱反应的化学方程式为 ▲ 。
(2)酸化时发生的反应为:2CrO42-+2H+![]() Cr2O72-+H2O,若1L酸化后所得溶液中含铬元素的质量为28.6 g,CrO42-有
Cr2O72-+H2O,若1L酸化后所得溶液中含铬元素的质量为28.6 g,CrO42-有![]() 转化为Cr2O72-。
转化为Cr2O72-。
①酸化后所得溶液中c(Cr2O72-)= ▲ ;
②已知:常温时该反应的平衡常数K=1014。上述酸化后所得溶液的pH=
▲ 。
(3)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7 mol·L-1以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①沉淀法:加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于 ▲ mol·L-1,后续废水处理方能达到国家排放标准。
②还原法:CrO42-![]() Cr3+
Cr3+ Cr(OH)3。用该方法处理10 m3 CrO42-的物质的量浓度为1.5×10—3mol·L-1的废水,至少需要绿矾(FeSO4·7H2O) ▲ kg。
Cr(OH)3。用该方法处理10 m3 CrO42-的物质的量浓度为1.5×10—3mol·L-1的废水,至少需要绿矾(FeSO4·7H2O) ▲ kg。
查看答案和解析>>
科目: 来源: 题型:
(12分)能源、材料和信息是现代社会的三大“支柱”。
(1)目前,利用金属或合金储氢的研究已取得很大进展,下图是一种镍基合金储氢后的晶胞结构图。
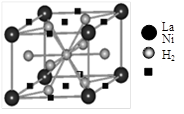
① Ni原子的价电子排布式是 ▲ 。
② 该合金储氢后,含1mol La的合金可吸附H2的数目为 ▲ 。
(2)南师大结构化学实验室合成了一种多功能材料——对硝基苯酚水合物(化学式为C6H5NO3·1.5H2O)。实验表明,加热至94℃时该晶体能失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
①晶体中四种基本元素的电负性由大到小的顺序是 ▲ 。
②对硝基苯酚水合物失去结晶水的过程中,破坏的微粒间作用力是 ▲ 。
(3)科学家把NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构。该阴离子的电子式是 ▲ ,其中心原子N的杂化方式是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com