
科目: 来源: 题型:
设NA为阿佛加德罗常数,下列说法不正确的是(相对原子质量Na:23 O:16 H:1)
A.78gNa2O2固体中含有的阴离子数为2NA
B.18g水中含有的电子数为10NA
C.常温常压下,金属钠从水中置换出22.4LH2,发生转移的电子数小于2NA
D.在1L2mol/L的硝酸铝溶液中含有的铝离子数为2NA
查看答案和解析>>
科目: 来源: 题型:
(13分) 某同学欲配制100mL0.20mol,L-1的KCl溶液,实验操作如下:
(A)用托盘天平准确称取1.49gKCl固体,并放入烧杯中;
(B)加入约30mL蒸馏水,用玻璃棒搅拌使其溶解,并恢复至室温;
(C)将KCl溶液由烧杯小心倒入100mL容量瓶中;
(D)然后往容量瓶中加蒸馏水,直到液面接近标线1-2cm处,轻轻摇动容量瓶并静置片刻后,改用胶头滴管滴加蒸馏水;
(E)使溶液凹面最低点恰好与刻度相切,把容量瓶盖好,上下翻转摇匀后装瓶。
(1)该学生操作中错误的是____ _____(填写编号)。
(2)下面哪些操作会导致所配的100mLO.20mol/L的KCl溶液浓度降低_ ___。
(A)容量瓶用蒸馏水洗涤三次直到洗净, (B)称量KCl固体时将砝码放在左盘
(C)未洗涤转移KCl溶液的烧杯, (D)转移KCl溶液时有KCl溶液溅出
(E)定容时仰视刻度线
(3)若用O.2mol,L-1的KCl溶液配制0.05mol,L-1的KCl溶液200.0mL,需要O.20mol,L-1的KCl溶液 mL,
(4)已知在标准状况下1L水可以溶解VLHCl气体,此时所形成的溶液密度为ρg/mL,(相对原子质量Cl35.5 H 1),该溶液物质的量浓度为: (mol/L)
查看答案和解析>>
科目: 来源: 题型:
(18分) 二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳
Ⅰ.①氧化产物是
②请写出化学反应方程式,并用单线桥法表示该反应的电子转移总数
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
①少量CO2通入过量的KOH溶液中,请写出离子反应方程式
②取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示
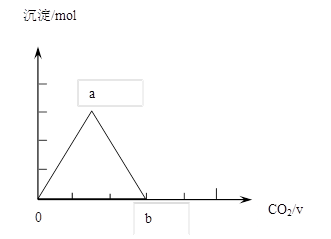

写出沉淀变化由a到b的离子方程式:
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系;并写出与图②中不同曲线处对应的离子反应方程式
查看答案和解析>>
科目: 来源: 题型:
有一透明溶液甲,欲确定是否含有下列离子: Na+、Mg2+、Al3+、Ba2+、SO、Cl-、I-、HCO,现取该溶液实验如下:
| 实验步骤 | 实验现象 |
| ①取少量甲溶液,滴加几滴甲基橙 | 溶液变红色 |
| ②取少量甲溶液,滴加Ba(NO3)2溶液 | 溶液无明显变化 |
| ③取②中实验后的溶液,滴加AgNO3溶液 | 有白色沉淀生成,且不溶于HNO3 |
| ④取少量甲溶液,滴加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
(1)由实验步骤①判断出溶液中肯定不存在的离子是 ,能说明这一实验事实的离子方程式是
(2)实验步骤③的实验结果说明溶液中不存在 离子
(3)欲确定的离子中肯定存在的是 。
(4)为进一步确定其他离子,应该补充的实验是
A.蒸发 B. 过滤 C.焰色反应 D. 渗析
查看答案和解析>>
科目: 来源: 题型:
(16分)某同学想通过下图装置实验、探究SO2与Na2O2反应的产物。
(夹持装置已略去,装置的气密性良好)
Ⅰ.装置B的作用是吸收水,干燥SO2气体,其原因是(用离子方程式表示)
。
装置D除了吸收过量的SO2,避免污染空气外,还起到的作用是
。
Ⅱ.某同学想通过上图实验装置,检验反应中是否有O2生成时,其实验操作步骤是:
① 先
②再用带火星的木条靠近干燥管口a,观察其是否复燃。
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3: 。
(1)若假设2成立,写出所发生反应的化学方程式
。
(2)若Na2O2反应完全,为确定C中固体产物的成分,甲设计如下实验:
得出结论:产物是Na2SO4。
该方案是否合理 (填“是”或“否”)。
(3)设计实验验证假设3的实验步骤如下:
| 实验步骤 | 实验现象 |
| ①滴加入过量的稀盐酸 | 产生剌激性气味气体 |
| ②滴加入适量的BaCl2溶液 | 产生白色沉淀。 |
| ③取少量C中固体产物于试管中,加入适量的蒸馏水溶解 |
|
若假设3成立,正确的实验操作顺序是
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.84gNaHCO3晶体中含有NA个CO32-
B.15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.4NA
C.标准状况下,11.2 L氯仿中含有的C-Cl键的数目为1.5NA
D.理论上氢氧燃料电池负极消耗11.2L标准状况下气体,外线路通过电子数为NA
查看答案和解析>>
科目: 来源: 题型:
水是最宝贵的资源之一。下列表述正确的是
A.H2O的电子式为![]()
B.4 ℃时,水的pH=7
C.D216O中,量数之和是质子数之和的两倍
D.273 K、101 kPa,2.4L水所含分子数约为6.02×1023
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式正确的是
A.用惰性电极电解MgCl2溶液: 2Cl‑ + 2H2O == Cl2↑+H2↑+2OH‑
B.硫化钠发生水解: S2‑+H2O = HS‑+OH‑
C.少量小苏打溶液滴入Ba(OH)2溶液中:HCO‑3 + Ba2+ +OH‑- = BaCO3↓+H2O
D.向NH4HSO4溶液中加入NaOH溶液至混合液为中性:H++OH‑= H2O
查看答案和解析>>
科目: 来源: 题型:
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g) +3H2(g) 2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.达平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
查看答案和解析>>
科目: 来源: 题型:
使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②用滴定管量取液体时,开始时平视读数,结束时俯视读数
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A.①③⑤⑥ B.①②⑤⑥ C.②③④⑥ D.③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com