
科目: 来源: 题型:
[化学——选修物质结构与性质](15分)
乙炔是有机合成工业的一种原料。工业上曾用![]() 与水反应生成乙炔。
与水反应生成乙炔。
(1)将乙炔通入 溶液生成
溶液生成![]() 红棕色沉淀。
红棕色沉淀。![]() 基态核外电子排布式为 。
基态核外电子排布式为 。
(2) Ca2+的原子结构示意图: ;已知![]() 中
中![]() 与
与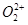 互为等电子体,
互为等电子体,![]() 的电子式可表示为 ;1mol
的电子式可表示为 ;1mol ![]() 中含有的
中含有的![]() 键数目为 。
键数目为 。
(3)乙炔与氢氰酸反应可得丙烯腈![]() 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
(4)![]() 晶体的晶胞结构与
晶体的晶胞结构与![]() 晶体的相似(如下图所示),但
晶体的相似(如下图所示),但![]() 晶体中含有的哑铃形
晶体中含有的哑铃形![]() 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。![]() 晶体中1个
晶体中1个![]() 周围距离最近的
周围距离最近的![]() 数目为 。
数目为 。
查看答案和解析>>
科目: 来源: 题型:
[化学——选修有机化学](15分)
相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
请根据所学知识与本题所给信息回答下列问题:
⑴ H的结构简式是 ;
⑵反应②、③的类型分别是 , 。
⑶ 反应⑤的化学方程式是______________________________ ______;
⑷ 阿司匹林最多消耗 mol NaOH;
⑸ 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 种;
⑹ 请用合成反应流程图表示出由A和其他无机物合成最合理的方案(不超过4步)。
例:

查看答案和解析>>
科目: 来源: 题型:
下列说法中,正确的是
① 同种元素的原子的性质相同
② 能自发进行的化学反应,不一定是△H<0 、△S>0
③ 胶体与溶液的本质区别是胶体具有丁达尔现象
④ Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关
⑤“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
⑥ 食盐可以融冰化雪,用食盐作融雪剂不会对环境、植物生长产生任何危害
⑦1 molNH2-中含电子数为9NA
A.①③④ B.①④⑥⑦ C.②⑤ D.①⑤⑦
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是
A.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
B.向碳酸氢镁溶液中加氢氧化钠溶液Mg2+ + 2HCO3- + 2OH- = MgCO3↓+CO32- + 2H2O
C.向100mL1mol/L的FeBr2溶液中通入 0.15molCl2 :
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
D.向明矾溶液逐滴加入Ba(OH)2溶液至Al3+离子刚好沉淀完全
Al3++SO42-+Ba2++3OH-=BaSO4↓+Al(OH)3↓
查看答案和解析>>
科目: 来源: 题型:
科学家合成了元素周期表上的第113号和第115号元素,第115号元素的![]() X原子在生成数微秒后会衰变成
X原子在生成数微秒后会衰变成![]() X。下列有关叙述中,正确的是
X。下列有关叙述中,正确的是
A.115号元素衰变成113号元素是化学变化
B.![]() X和
X和![]() X是两种核素
X是两种核素
C.![]() X的中子数与质子数之差为174
X的中子数与质子数之差为174
D.113号元素位于周期表第八周期
查看答案和解析>>
科目: 来源: 题型:
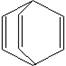
桶烯(Barrelene)结构简式如右图所示,则下列有关说法不正确的是
A.桶烯中的一个氢原子被氯原子取代,所得产物只有两种
 B.桶烯在一定条件下能发生加成反应和加聚反应
B.桶烯在一定条件下能发生加成反应和加聚反应
C.桶烯与苯乙烯(C6H5CH=CH2)互为同分异构体
D.桶烯分子中所有原子在同一平面内
查看答案和解析>>
科目: 来源: 题型:
把在空气中久置的铝片5.0 g投入盛有 500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如右的坐标曲线来表示:
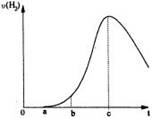 下列推论错误的是
下列推论错误的是
A.t由0→a段不产生氢气是因为铝的表面存在一层致密的
氧化膜
B.t由b→c段产生氢气的速率增加较快的主要原因之一是
温度升高
C.t=c时反应处平衡状态
D.t>c产生氢气的速率降低主要是因为溶液中c(H+)降低
查看答案和解析>>
科目: 来源: 题型:
室温下,在25mL0.1mol•L-1 NaOH溶液中逐滴加入0.2 mol • L-1 CH3COOH溶液,pH 与滴加 CH3COOH 溶液体积的关系曲线如右图所示,若忽略两溶液混合时的体积变
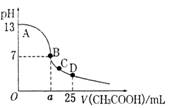 化,下列有关粒子浓度关系的说法错误的是
化,下列有关粒子浓度关系的说法错误的是
A.在A、B间任一点,溶液中一定都有
B.在B点:a>12.5,且有
C.在C点:
D..在D点:
查看答案和解析>>
科目: 来源: 题型:
已知可逆反应:A(s)+2B(g)C(g)+D(g) △H<0。在一定温度下将1mol A和2molB加入如右图所示甲容器中,将2 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,在恒温下使两容器内反应均达到平衡状态(如图所示,隔板K不能移动)。下列说法正确的是
A.保持乙中压强不变 ,升高温度,达到新的平衡后,乙中平均相对分子质量增大
B.保持温度和乙中压强不变 ,向乙中再加入2 mol D,达到新平衡后,一定有c(B)乙>c(B)甲
C.若该温度下反应的K=1,则甲中B和乙中C的转化率均为66.7%
D.保持温度和活塞位置不变,甲中再加入1 mol A和2mol B,达到新的平衡后,c(B)甲=2c(B)乙
查看答案和解析>>
科目: 来源: 题型:阅读理解
(15分)
Ⅰ.(6分)光合作用是由二氧化碳与水合成葡萄糖,同时放出氧气。设想将该反应倒过来,可设计成一个原电池,产生电流,这样就将太阳能转变成了电能。
(1)写出该原电池的总反应式:______________________________________
(2)写出该电池在酸性介质中放电的电极反应式:
负极:_____________________________________________
正极:_____________________________________________
Ⅱ.(6分)类比思维是学习化学的重要方法,但结果是否正确必须经受检验。在进行类比思维的时候,不能机械类比,一定要注意一些物质的特殊性,以防止类比出错误的结论。凭已有的化学知识,下列类比结果正确的是:(填标序号) 。若错误,在其后写出正确的。
①在相同条件下,Na2CO3溶解度比NaHCO3大
类比:在相同条件下,CaCO3溶解度比Ca(HCO3)2大
正确的应该为(若类比正确,此处不写,下同。): 。
②向次氯酸钙溶液中通过量CO2:CO2 +ClO- + H2O = HCO3- + HClO
类比:向次氯酸钠溶液中通过量SO2:SO2 + ClO- + H2O= HSO3- + HClO
正确的应该为: 。
③根据化合价Fe3O4可表示为:FeO·Fe2O3 类比:Fe3I8也可表示为FeI2·2FeI3
正确的应该为: 。
④CaC2能水解:CaC2+2H2O =Ca(OH)2 + C2H2↑
类比:Al4C3也能水解:Al4C3 + 12H2O = 4Al(OH)3↓+ 3CH4↑
正确的应该为: 。
Ⅲ.(3分)常温下,某水溶液M中存在的离子有:Na+、A-、H+、OH-。若该溶液M由 pH=3的HA溶液![]() mL与pH=11的NaOH溶液
mL与pH=11的NaOH溶液![]() mL混合反应而得,则下列说法中正确的是 (填字母)。
mL混合反应而得,则下列说法中正确的是 (填字母)。
A.若溶液M呈中性,则溶液M中C(H+)+C(OH-)=2×10-7mol·L-1
B.若V1=V2,则溶液M的pH一定等于7
C.若溶液M呈酸性,则V1一定大于V2
D.若溶液M呈碱性,则V1一定小于V2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com