
科目: 来源: 题型:
(12分)
A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如下所示:
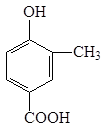



A B C D
(1)A中的含氧官能团名称是 。
(2)B与足量氢气充分反应的产物的结构简式为 。
(3)D发生聚合反应的产物的结构简式为 。
(4)A能与乙醇发生反应生成一种有特殊香味的物质,请写出该反应的方程式:
。
(5)关于上述四种物质的说法中正确的是 。
A.都能与Na反应放出H2
B.C、D均能使溴的四氯化碳溶液褪色
C.A和C均能与NaHCO3溶液反应放出CO2
D.1molC最多能与4molBr2发生反应
查看答案和解析>>
科目: 来源: 题型:
(13分)
 甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
①CH4(g)+H2O(g) CO(g)+3H2(g) △H1
②CO(g)+2H2(g) CH3OH(g) △H2
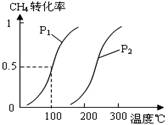
将0.20mol CH4和0.30 mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如右图。
(1)温度不变,缩小体积,增大压强,①的反应速率 (填“增大”、“减小”或“不变”),平衡向 方向移动。
(2)反应①的△H1 0(填“<”、“=”或“>”),其平衡常数表达式为K= ,100℃时的平衡常数值是 。
(3)在压强为0.1 MPa条件下, 将a mol CO与 3a mol H2的混合气体在催化剂作用下进行反应②生成甲醇。为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。请在下表空格中填入剩余的实验条件数据。
| 实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) |
| I | 150 | 1/3 | 0.1 |
| II |
|
| 5 |
| III | 350 |
| 5 |
查看答案和解析>>
科目: 来源: 题型:
(12分)
现代循环经济要求综合考虑环境污染和经济效益。请填写下列空白。
(1)实验室里,可用于吸收SO2尾气的一种试剂是 。
(2)高纯氧化铁可作现代电子工业材料。以下是用硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、 FeO、SiO2)为原料制备高纯氧化铁(软磁α- Fe2O3)的生产流程示意图:

①步骤I中过滤所得滤渣的主要成分是 。
②步骤II中加入铁粉的目的是 。
③步骤Ⅲ中可选用 试剂调节溶液的pH(填标号)。
A.稀硝酸 B.双氧水 C.氨水 D.高锰酸钾溶液
④写出在空气中煅烧FeCO3,制备高纯氧化铁的化学方程式 。
⑤从滤液C中回收的主要物质的一种用途是 。
查看答案和解析>>
科目: 来源: 题型:
(12分)
实验室需要制备纯净的氯化钾。现有含少量KBr和K2SO4的氯化钾样品,按照下图所示的实验方案进行提纯。

(1)过滤时需要用到的玻璃仪器是 。
(2)检验加入BaCl2溶液后SO42-是否沉淀完全的操作为 。
(3)若用硝酸钡来代替氯化钡,请判断是否可行,并说明理由 。
(4)某同学认为该实验方案中加适量氯化钡溶液不容易控制,应加入过量氯化钡溶液。
他的思路如下:
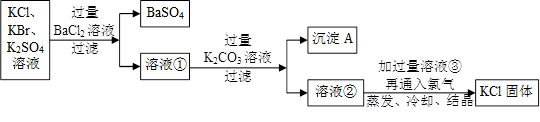
沉淀A的化学式是 ,溶液③中的溶质是 。
查看答案和解析>>
科目: 来源: 题型:
(12分)
钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一。
(1)请写出工业上用电解方法制取钠的化学方程式 。
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是 。
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质。
①提出合理假设。
假设1:该漂白粉未变质,只含 ;
假设2:该漂白粉全部变质,只含 ;
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3。
② 设计实验方案,进行实验。请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-,表格可以不填满。)
| 实验步骤 | 预期现象和结论 | |
| ① | 取少量上述漂白粉于试管中,
|
|
| ② |
|
|
| ③ |
|
|
查看答案和解析>>
科目: 来源: 题型:
从日本福岛核电站泄漏的放射性物质中,大量存在一种叫做“碘一13l”的放射性元素。下列关于13155I和12755I的说法正确的是 ( )
A.13155I和12755I都含有55个中子
B.13155I和12755I互为同位素
C.13155I和12755I的核外电子数不同
D.13155I和12755I分别含有131和127个质子
查看答案和解析>>
科目: 来源: 题型:
NA表示阿伏伽德罗常数,下列判断正确的是 ( )
A.标准状况下,1L液态水中含有的H+数目为10-7NA
B.常温常压下,16g CH4中的分子数为NA
C.1L 0.2mol/L的FeCl3溶液中Fe3+的数目为0.2NA
D.含NA个Na+的Na2O溶解于lL水中,Na+的物质的量浓度等于1 mol/L
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式书写正确的是 ( )
A.含1molFeCl2的溶液中通入1molCl2 Fe2++Cl2=Fe3++2Cl-
B.NaClO溶液中通入过量的SO2气体 ClO-+SO2+H2O HClO+HSO3一
C.在足量热的稀硫酸中不断通入空气氧化废铜 2Cu+O2+4H+=2Cu2++2H2O
D.工业上将硫酸工业尾气SO2持续通入氨水中 SO2+OH-=HSO3一
查看答案和解析>>
科目: 来源: 题型:
某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是 ( )
A.正极反应式为:O2+2H2O+4e- 4OH—
B.工作一段时间后,电解液中的KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2 2H2O
D.放电过程中,溶液中K+向负极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com