
科目: 来源: 题型:
将电极A与B插入电解液里,发现电极A质量减少,B质量增加,符合这一情况的是( )
A. 电解液是稀硫酸 B. A和B均为石墨电极
C. A是阴极,B是阳极 D. A和B均为铜电极
查看答案和解析>>
科目: 来源: 题型:
下列选项所述的两个量中,前者一定大于后者的是( )
A. 在80℃和25℃时,纯水的pH值
B. 常温常压下,HF和HCl的沸点
C. 常温常压下,CO2与Cl2在水中的溶解度
D. 等浓度的CH3COOH与CH3COONa溶液中的c(CH3COO-)
查看答案和解析>>
科目: 来源: 题型:
下列各项中的两个量,其比值一定为2:1的是( )
A. 在密闭容器中,N2+ 3H2 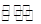 2NH3达到平衡时的c(NH3)与c (N2)
2NH3达到平衡时的c(NH3)与c (N2)
B. 0.1 mol / L Na2CO3溶液中的c (Na+)与c (CO32-)
C. 在反应2 H2S+ SO2 → 3 S + 2 H2O中被氧化与被还原的硫原子的质量
D. 相同温度下,0.2 mol/ L 醋酸溶液与0.1 mol / L 醋酸溶液中的c(H+)
查看答案和解析>>
科目: 来源: 题型:
某无色溶液,由Na+、Ba2+、Al3+、AlO2-、Fe3+、CO32-、SO42-中的若干种组成。取适量该溶液进行如下实验:① 加入过量盐酸,有气体生成;②在 ① 所得溶液中再加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;③ 在 ② 所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。原溶液中一定存在的离子是( )
A. Al3+ 、Fe3+ 、SO42- B. Na+ 、 AlO2- 、SO42- 、CO32-
C. Na+、 AlO2-、 CO32- D. Na+、Ba2+、 AlO2-
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数,下列说法正确的是( )
A. 标况下,5.6 L乙烯和丙烯的混合气体中含有0.25 NA个碳碳双键
B. 0.05 mol熔融的KHSO4中含有阳离子数目为0.10 NA
C. 6.4 g CaC2晶体中含有的阴阳离子总数为0.3 NA
D. 电解饱和NaCl溶液,转移0.1 NA个电子时阳极得到0.1 g H2
查看答案和解析>>
科目: 来源: 题型:
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g) + O2(g) ![]() 2SO3 (g),并达到平衡。在此过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为P%,则乙容器中SO2的转化率( )
2SO3 (g),并达到平衡。在此过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为P%,则乙容器中SO2的转化率( )
A. 等于P% B. 小于P % C. 大于P% D. 无法判断
查看答案和解析>>
科目: 来源: 题型:
有Na2CO3、NaHCO3、CaO和NaOH组成的混合物27.2克,把它们溶于足量的水中,充分反应后溶液中的Ca2+、CO32-、HCO3-均转化为沉淀。将反应容器内水分蒸干,得到白色固体物质共29克,则原混合物中Na2CO3的质量为( )
A.10.6克 B.5.3克 C. 5.9克 D. 无法确定
查看答案和解析>>
科目: 来源: 题型:
室温下,某无色溶液中由水电离出来的H+和OH-浓度的乘积为10-24,则此溶液中可能大量共存的离子组是( )
A. HCO3-、Al3+、Na+、SO42- B. I-、NO3-、K+、NH4+
C. MnO4-、Cl-、SO42-、K+ D. SiO32-、SO32-、Na+、Cl-
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,固定容积的密闭容器中反应:2NO2(g)![]() O2(g) + 2NO(g) —Q(Q>0),达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是( )
O2(g) + 2NO(g) —Q(Q>0),达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是( )
A.当X表示温度时,Y表示NO2的物质的量
B.当X表示压强时,Y表示NO2的转化率
C.当X表示反应时间时,Y表示混合气体的密度
D.当X表示NO2的物质的量时,Y表示O2的物质的量
查看答案和解析>>
科目: 来源: 题型:
取0.2 mol / L HX溶液与0.2 mol / LNaOH溶液等体积混合(忽略混合后溶液体积变化),测得混合溶液的pH = 8,则下列说法正确的是( )
A.混合溶液中由水电离出的c (OH-)小于0.2 mol / LHX溶液中由水电离出的c(H+)
B. c (Na+) = c (X-) +c (HX) = 0.2 mol / L
C. c (Na+) — c (X-) =9.9×10-7mol /L
D. c (OH-) — c (HX) = c(H+)= 10-8 mol / L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com