
科目: 来源: 题型:
以水为溶剂进行中和滴定的原理是:H3O++OH-=2H2O.已知液态SO2和纯水的导电性相近,因为液态SO2也会发生自离解:SO2(l)+SO2(l)SO32-+SO2+.若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是 ( )
A.该滴定反应可以表示为:SO32- + SO2+=2SO2
B.在一定温度下,液态SO2中c(SO32-)与c(SO2+)的乘积是一个常数
C.自离解的存在,说明SO2是离子化合物
D.可通过导电能力变化来判断是否到达滴定终点
查看答案和解析>>
科目: 来源: 题型:
(6分)(1).中和pH=3的醋酸(Ka=1.75×10-5)100mL,需要0.1mol/LNaOH溶液的体积为:____________.
(2).在一定体积0.005mol/LBa(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH = 11.假设反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是______________.
查看答案和解析>>
科目: 来源: 题型:
(6分)今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Cl-、Cu2+、Fe3+、CO32—、SO42—,现每次取100.00ml进行下列实验:
①第一份加入AgNO3溶液有沉淀产生.
②第二份加足量NaOH后加热,收集到气体0.896L(标准状态下).
③第三份加足量BaCl2后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩余2.33g.在原溶液中一定存在的离子及其物质的量浓度分别为: _______________ .
查看答案和解析>>
科目: 来源: 题型:
(12分)由短周期元素组成的A、B两种盐可发生下列变化,且B的焰色反应呈黄色(图中其它生成物未列出)
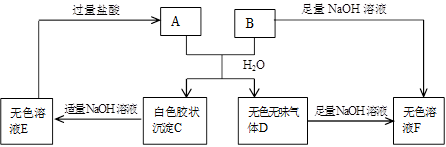
(1)A和B的混合物溶于水发生反应的离子方程式______________________________.
(2)B、E两溶液混合反应时,可观察到的现象是__________________________,写出其反应的离子方程式__________________________________________________.
查看答案和解析>>
科目: 来源: 题型:
(13分)茶是我国人民喜爱的饮品,其中含有多种有益于人体健康的成分,据测定茶叶中含有450种以上的有机成分与15种以上的元素.某化学研究小组欲探究茶叶中钙元素的含量,设计了探究实验方案如下:(已知茶叶中的铝、铁元素对钙离子的测定有影响)
步骤1:称取500 g干燥的茶叶,置于通风橱中,充分灼烧使茶叶灰化,再用研钵磨细后移入烧杯中,然后将200mL 1 mol·L-1盐酸加入灰中搅拌、过滤、洗涤.
步骤2:向步骤1所得滤液中逐滴加入稀氢氧化钠溶液,调节溶液的pH为6~7左右,使铝、铁的氢氧化物完全沉淀,再加热煮沸30 min,加入7.95 g无水碳酸钠,充分搅拌,待沉淀完全后,过滤,洗涤,过滤后得到滤液和沉淀.
步骤3:将步骤2所得的滤液稀释至500 mL,取其中的20.00 mL溶液以甲基橙作指示剂,用0.1000 mol·L-1的HCl标准溶液滴定,终点时消耗盐酸的体积为20.00 mL,计算结果.请回答下列问题:
步骤 1中:使茶叶灰化需要三角架、泥三角、酒精喷灯、_________、_________等仪器.
步骤2中:改用试剂________________来调节pH将更为方便.判断沉淀已经洗涤干净的方法是______________________________________________________________.
步骤3中:原茶叶中钙离子的质量分数为________________.若碳酸钠试剂不纯,且所含杂质不与Ca2+反应,则测得的钙离子的质量分数将__________(填下列序号之一:①偏小 ②偏大 ③不偏 ④偏小或偏大或不偏)
查看答案和解析>>
科目: 来源: 题型:
(8分)化合物SOCl2是一种液态化合物,沸点为77℃,在盛有10mL的锥形瓶中小心滴加8~10滴SOCl2,可观察到剧烈水解反应,液面有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色.轻轻振荡锥形瓶,等白雾消失后,往溶液中滴加AgNO3溶液,有不溶于HNO3的白色凝乳状沉淀析出.
(1)根据上述实验,写出SOCL2和水反应的化学方程式 __.
(2)AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3·H2O混合共热,可得到无水AlCl3,其原因是 __________________________ __________________.
查看答案和解析>>
科目: 来源: 题型:
我们可以通过以下实验步骤来验证醋酸银(CH3COOAg)的溶度积KSP=2.0×10-3:将已知质量的铜片加入到CH3COOAg饱和溶液中(此饱和溶液中没有CH3COOAg固体),待充分反应之后,将铜片冲洗干净、干燥、称重.
(1)写出表示CH3COOAg沉淀溶解平衡的方程式.
(2)刚开始铜片的质量为23.4 g,将铜片放在100 mL的CH3COOAg饱和溶液中,通过计算说明当充分反应后铜片的质量为何值时,CH3COOAg的KSP=2.0×10-3可以得到证实.( ![]() =2.24,
=2.24, ![]() =1.41)
=1.41)
查看答案和解析>>
科目: 来源: 题型:
下列哪一项符合“绿色化学”的原则
A.排放前对废气、废水、废渣进行无害化处理
B.在化学生产中少用或不用有害物质以及少排放或不排放有害物质
C.在化工生产中,尽量避免使用任何化学物质
D.在化工厂范围多种草种树,努力构建花园式工厂
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是
A.钢、青铜、硬铝和金刚石都是合金材料
B.所有的分解反应都属于氧化还原反应
C.氨基酸不能通过缩聚反应结合成蛋白质
D.一定条件下,稻草可制得葡萄糖或酒精
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com