
科目: 来源: 题型:
下列说法中正确的是
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C.最外层有2个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
查看答案和解析>>
科目: 来源: 题型:
X、Y是元素周期表ⅦA族中的两种元素。下列叙述中不能说明X的非金属性比Y强的
A.X气态氢化的酸性比Y的气态氢化物的酸性强
B.惰性电极电解NaX和NaY的混合液时,先产生Y2
C.X的气态氢化物比Y的气态氢化物稳定
D.X的单质能将Y从NaY的溶液中置换出来
查看答案和解析>>
科目: 来源: 题型:
某同学按右图所示的装置进行电解实验。下列说法正确的是
![]()
A.电解过程中,铜电极上有H2产生
B.电解初期,主反应方程式为:Cu+H2SO4 CuSO4+H2↑
C.电解开始时,石墨电极上有铜析出
D.整个电解过程中,H+的浓度不断增大
查看答案和解析>>
科目: 来源: 题型:
用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一种物质(括号内),溶液能与原来溶液完全一样的是
A.CuCl2[CuSO4] B.NaOH[NaOH] C.NaCl [HCl] D.CuSO4 [Cu(OH)2]
查看答案和解析>>
科目: 来源: 题型:
10分)按下图装置进行实验,并回答下列问题
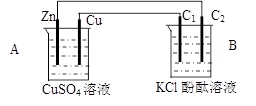
⑴判断装置的名称:A池为 B池为
⑵锌极为__________极,电极反应式为
铜极为__________极,电极反应式为
石墨棒C1为______极,电极反应式为_______________
石墨棒C2附近发生的实验现象为_______________________________
⑶当C2极析出224mL气体(标准状态时),锌的质量变化 (增加或减少)_________g,CuSO4溶液的质量变化 (增加或减少了)_________g
查看答案和解析>>
科目: 来源: 题型:
(11分)
Ⅰ.(8分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)若知上述反应每产生2.24LCO气体(折为标准状况)放出QkJ的热量,则其热化学方程式为
(3)用轨道表示式表达Si 核外电子排布情况
(4)已知Si的电负性为1.8 ,H的电负性为2.1,N的电负性为3.0 ,则SiH4 中硅的化合价为 ,Si3N4所属的化合物类型是 (填离子化合物or共价化合物),在前四周期的元素中,未成对电子数最多的元素的电子排布式为
Ⅱ.(3分)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
2N2(g)+CO2(g)+2H2O(g)=CH4(g)+4NO(g) ΔH=+1160 kJ·mol-1
若用标准状况下4.48LCH4还原NO2至N2 ,整个过程中转移的电子总数为 (阿伏伽德罗常数用NA表示),放出的热量为 kJ。
查看答案和解析>>
科目: 来源: 题型:阅读理解
(10+6分)有一研究性学习小组在探究有关钢铁的腐蚀情况,他们进行了如下实验:在一个水槽中盛装1000 mL水,加入一定量的NaCl固体溶解后通入SO2 气体至溶液pH值约为4左右,另取一支试管(带刻度,规格50mL),一条约5cm 的细铁丝,将铁丝放入试管中,加入 约 10mL前面配好的溶液,迅速用拇指扣住试管口倒扣于水槽中,用铁架台将试管固定,如右下图。过一会儿:

(1)观察到试管中的液面逐渐下降,这说明
在该条件下,铁丝发生了 腐蚀,
正极材料是 电极反应是
(2)再过一段时间发现液面停止下降,并且开始逐渐
上升,露在液面上的铁丝表面由原来的银白色变棕褐色,这说明在该条件下,铁丝发生了
腐蚀,正极的电极反应为
①总反应为: ;① 反应的产物极易被进一步氧化,生成红褐色物质,② 该反应的化学方程式为: 若铁锈的组成为:Fe2O3·xH2O ,试写出由②反应的产物在通常条件下生成铁锈的反应方程式:
③
附加题(6分)(3)已知原来铁丝质量为2 g,发生(1)情况时,依液面下降的高度折为标准状况下的体积是5.6mL,则此时,铁丝的质量变为 g ,随后液面开始上升,即发生(2)的变化,依最终液面上升的高度折算为标准状况下的体积比最开始刚倒扣于水槽中试管中溶液的体积多了1.12mL,通过计算,(2)的过程共消耗氧气 mL,若x值为2,那么铁丝的质量应为 g(以上计算有效数字保留至小数点后三位)
查看答案和解析>>
科目: 来源: 题型:
(12分)X、Y、Z、L、M五种元素的原子序数依次增大。X、Y是组成有机物的基本元素,Z的最外层电子分布情况是P轨道上的电子比S轨道上的电子多一个,L在所有元素中电负性排第二位,其原子最外层有两个未成对电子,M的正三价离子其核外第三电子层有五个未成对电子。回答下列问题:
⑴ L的元素符号为 ;M在元素周期表中的位置为 ;五种元素的原子半径从大到小的顺序是 (用元素符号表示)。
⑵ Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为 ,B—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,B—空气燃料电池放电时:负极的电极反应式是: 。
⑶ 硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的特征构型的电子排布式为 ,其最高价氧化物对应的水化物化学式为 。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+99.7kJ·mol-1 b.+29.7 kJ·mol-1 c.-20.6 kJ·mol-1 d.-241.8 kJ·mol-1
⑷ 用M单质作阳极,石墨作阴极,NaOH 溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式: ;
查看答案和解析>>
科目: 来源: 题型:
(9分)某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:
【实验1】:如右下图装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细。电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10。随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,溶液始终未出现蓝色。
【实验2】:将实验1中试管底部的橙黄色沉淀取出,分装在两
支小试管中,以后的操作和现象如下:
| 序号 | 操作 | 现象 |
| ① | 滴入稀硝酸溶液 | 沉淀溶解,有无色气泡产生,最终得到蓝色溶液。 |
| ② | 滴入稀硫酸溶液 | 橙黄色沉淀转变为紫红色不溶物,溶液呈现蓝色 |
阅读资料:常见铜的化合物颜色如下:
| 物质 | 颜色 | 物质 | 颜色 |
| 氯化铜 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 氢氧化亚铜 (不稳定) | 橙黄色 |
| 碱式氯化铜 | 绿色 | 氢氧化铜 | 蓝色 |
| 氧化亚铜 | 砖红色或橙黄色 | 氯化亚铜 | 白色 |
请回答下列问题:
(1)铜的常见正化合价为________、_______,最终试管底部橙黄色沉淀的化学式_______________。
(2) 电解开始30s内,阴极上发生的反应为: 、阳极上发生的反应为: 。
(3)写出实验2中①、②的离子方程式:①_______________;②___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com