
科目: 来源: 题型:
在6KOH + 3Cl2 == KClO3 + 5KCl + 3H2O的反应中,下列说法中正确的是
A.KCl是还原产物,KClO3是氧化产物
B.Cl2是氧化剂,KOH是还原剂
C.KOH是氧化剂,Cl2是还原剂
D.被氧化的氯原子与被还原的氯原子数之比为1∶5
查看答案和解析>>
科目: 来源: 题型:
下列关于等物质的量的碳酸钠和碳酸氢钠的比较中,正确的是
A.二者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠的溶解度
B.二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠的热稳定性
C.二者都能与盐酸反应放出二氧化碳气体,但产气量和反应快慢不同
D.二者在一定的条件下可以相互转化
查看答案和解析>>
科目: 来源: 题型:
(4分)下列4组物质均有一种物质的类别与其它3种不同,请找出并填在下面空格。
A.CaO、Na2O、CO2、CuO B.C、Na、Mg、Al
C.Na2CO3、FeSO4、Cu(NO3)2、KOH D.H3PO4、H2O、H2SO4、HNO3
以上四组物质中与其他三个不同的物质依次是(填化学式)
A ;B ;C ;D 。
查看答案和解析>>
科目: 来源: 题型:
(5分)A、B、C、D四种化合物,其中A、C、D焰色反应均为黄色,而B的焰色反应为紫色,A、C和盐酸反应均得到D,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,若B的溶液滴加到硫酸亚铁溶液会先后出现白色沉淀→灰绿色沉淀→红褐色沉淀E。试推断:
A: 、B: 、C:_________、D:_________、E:
查看答案和解析>>
科目: 来源: 题型:
(8分)现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:

请回答下列问题:
⑴写出实验流程中下列物质的化学式:试剂X: ,沉淀A: ,沉淀B: 。
⑵上述实验流程中加入过量的Na2CO3的目的是 。
⑶按此实验方案得到的溶液3中肯定含有 杂质(填化学式);为了解决这个问题,可以向溶液3中加入适量的 ,之后若要获得固体NaNO3需进行的实验操作是 (填操作名称)。
查看答案和解析>>
科目: 来源: 题型:
(6分)在AlCl3溶液中,逐滴滴入NaOH溶液,刚开始可以观察到 ,写出有关的化学方程式 ,继续往溶液中滴入NaOH溶液,可以观察到 ,写出有关的离子方程式 。
查看答案和解析>>
科目: 来源: 题型:
(14分)在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。请回答该实验中的问题。
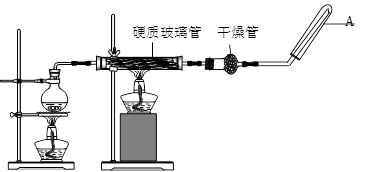
(1)写出该反应的反应方程式 ;并指明该氧化还原反应的还原剂是 (填化学式,下同),氧化剂是 。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;烧瓶底部放置了几片碎瓷片,其作用是 。
(3)试管中收集气体是 (填化学式),如果要在A处玻璃管处点燃该气体,则必须对该气体进行 。
(4)该同学欲确定反应后硬质试管中还原铁粉是否完全反应,其中的固体成分有哪些,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质一定有 ,若溶液未变红色则说明硬质试管中固体物质的成分是 。
(5)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是(用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
(7分)某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数。可供选用的试剂有:浓H2SO4、浓硝酸、6 mol·L-1 NaOH溶液。

请填写下列空白:
(1)有关实验操作:a、往试管中放入适量的铝合金样品;b、从分液漏斗往试管中加入过量的A溶液;c、检查装置的气密性;d、测定收集到的水的体积。
正确的操作顺序为_______________________________(填字母)。
(2)A溶液可选用___________________________________________
(3)写出实验中发生反应的化学方程式:_________________________________________。
(4)若实验中测得样品的质量为Wg ,氢气的体积为a L(标准状况),则样品中Al的质量分数为_ __。
查看答案和解析>>
科目: 来源: 题型:
(6分)将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)求:

(1)生成沉淀达到最大时消耗NaOH的物质的量___________mol
(2)合金中Mg的质量________g
(3)所用HCl的物质的量浓度为__________。
查看答案和解析>>
科目: 来源: 题型:
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13mL稀盐酸 B.用pH计测得某稀盐酸的pH为1.54
C.用碱式滴定管量取20.3 mL烧碱溶液 D.用托盘天平称得某物质的质量为13.15g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com