
科目: 来源: 题型:单选题
| 现象 | 解释 | |
| A | 浓硫酸在光照下颜色变黄 | 浓硝酸不稳定 |
| B | 浓硫酸可使pH试纸先变红后变黑 | 浓硫酸具有酸性和吸水性 |
| C | 向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中含有SO |
| D | Cl2和SO2均可使含有酚酞的NaOH溶液褪色 | Cl2和SO2均具有漂白性 |
查看答案和解析>>
科目: 来源: 题型:单选题
| 生成CaCO3 | 溶液中HCO3- | H2 | 转移的电子 | |
| A | 0.1NA | 0.1NA | ||
| B | 11.2L | 0.1NA | ||
| C | 10g | 0.1NA | ||
| D | 10g | 0.05NA |
查看答案和解析>>
科目: 来源: 题型:单选题
 SiO32-+H2O
SiO32-+H2O查看答案和解析>>
科目: 来源: 题型:解答题
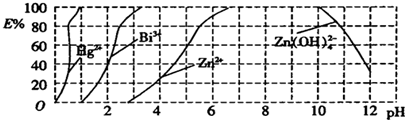
 络合萃取法处理废水.
络合萃取法处理废水.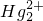 )必须转换成汞离子(Hg2+)才能用双硫腙络合.某工厂污水中含有较多的氯化亚汞(Hg2Cl2),加入二硫酸钾(K2S2O8)可氧化
)必须转换成汞离子(Hg2+)才能用双硫腙络合.某工厂污水中含有较多的氯化亚汞(Hg2Cl2),加入二硫酸钾(K2S2O8)可氧化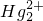 ,写出该反应的化学方程式:______.
,写出该反应的化学方程式:______.查看答案和解析>>
科目: 来源: 题型:解答题
 某同学设计如图所示装置分别进行探究实验(夹持装置已略去)
某同学设计如图所示装置分别进行探究实验(夹持装置已略去)| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| ① | Cu、稀HNO3 | H2O | |
| ② | NaOH固体、浓氨水 | NH3 | |
| ③ | Na2CO3固体、稀H2SO4 | CO2 | |
| ④ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| 1 | 1.0g | 10.0mL | 347.5mL |
| 2 | 1.0g | 10.0mL | 335.0mL |
| 3 | 1.0g | 10.0mL | 344.5mL |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
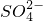 来判断沉淀是否洗涤干净.检验
来判断沉淀是否洗涤干净.检验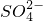 操作是______
操作是______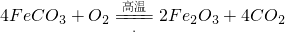 ,现煅烧464.0kg的FeCO3,得到316.8kg产品,若产品中杂质只有FeO,则该产品中Fe2O3的质量是______kg(摩尔质量/g?mol-1:FeCO3-116 Fe2O3-160 FeO-72)
,现煅烧464.0kg的FeCO3,得到316.8kg产品,若产品中杂质只有FeO,则该产品中Fe2O3的质量是______kg(摩尔质量/g?mol-1:FeCO3-116 Fe2O3-160 FeO-72)查看答案和解析>>
科目: 来源: 题型:解答题
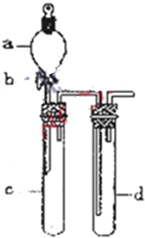 铜与浓硝酸反应和铜与稀硝酸反应,产物不同,实验现象也不同.某课外活动小组为了证明并观察到铜与稀硝酸反应的产物为NO,设计了如图所示的实验装置.请你根据他们的思路,选择下列药品,完成该实验,并叙述实验步骤.药品:稀硝酸、盐酸、Zn粒、CaCO3固体
铜与浓硝酸反应和铜与稀硝酸反应,产物不同,实验现象也不同.某课外活动小组为了证明并观察到铜与稀硝酸反应的产物为NO,设计了如图所示的实验装置.请你根据他们的思路,选择下列药品,完成该实验,并叙述实验步骤.药品:稀硝酸、盐酸、Zn粒、CaCO3固体查看答案和解析>>
科目: 来源: 题型:多选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com