
科目: 来源: 题型:
下列叙述错误的是
![]() A. 在周期表中位置相同,都在第4纵行
A. 在周期表中位置相同,都在第4纵行
B.CO2的分子模型:
C.在CS2、PCl3中各原子最外层均能达到8电子的稳定结构
D.HF、HCl、HBr、HI的稳定性依次增强
查看答案和解析>>
科目: 来源: 题型:
下列说法错误的是
A.在化合物 中,存在手性碳原子
B. 原子间形成分子时,决定各原子相互结合的数量关系的是共价键的饱和性?
C.根据对角线规则判断Be(OH)2是两性氢氧化物
D.在相同条件下,邻羟基苯甲醛的沸点高于对羟基苯甲醛
查看答案和解析>>
科目: 来源: 题型:
根据下表信息,判断以下叙述正确的是
表 部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目: 来源: 题型:
主族元素X的原子最外电子层中具有最多的未成对电子,元素Y的原子只有两种形状的电子云,且两种电子云的电子数相等,则X、Y组成的微粒中,不可能存在的是
A.X2Y5 B.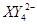 C.
C.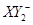 D.
D.
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)B的氢化物的分子空间构型是 。其中心原子采取 杂化。
(2)写出化合物AC2的电子式 。AC2是由 键组成的 (填“极性”或“非极性”)分子。
(3)E的外围电子排布式是 ,在形成化合物时它的最高化合价为 , ECl3形成的配合物的化学式为 。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。
查看答案和解析>>
科目: 来源: 题型:
下表为元素周期表的一部分,请参照元素A-H在表中的位置,
| 族 周期 | IA |
| 0 | |||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
|
| 2 |
|
|
| B | C | D |
|
|
| 3 | E |
| F | G |
|
| H |
|
用化学用语回答下列问题:
(1)D、E、F的原子半径由大到小的顺序为_________________________。
(2)B、C、D的第一电离能由大到小的顺序为_________________________。
(3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4) E、F的最高价氧化物的水化物相互反应的离子方程式 。
(5)在B所形成的化合物CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有 ;
与CO分子互为等电子体的分子和离子分别为 和 ,根据等电子理
论推测CO分子的结构式可表示成 ,一个CO分子中有 个σ键, 个л键。
(6)根据VSEPR理论预测D和H所形成的HD4—离子的空间构型为______________型。
(7)由A、B、C、D、E元素组成的10电子粒子中,含配位键的有 、 ;
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为:,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A _________ B__________ C __________ D__________
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是__________,碱性最强的是_________。
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是__________,电负性最大的元素是__________。
(4)E元素原子的核电荷数是__________,E元素在周期表的第_______周期,第________族,已知元素周期表可按电子排布分为s区、p区等,则E元素在_______区。;E与CO易形成配合物E(CO)5,在E(CO)5中E的化合价为__________
(5)画出D的轨道表示式__________________________________________,这样排布遵循了____________原理和____________规则。
(6)用电子式表示B的硫化物的形成过程:___________________________________
查看答案和解析>>
科目: 来源: 题型:
2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想。运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物。已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键。
(1)该氮氢化合物的结构式为 。
(2)若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,写出该反应的化学方程式 。
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl。试写出
上述氮氢化合物通入足量盐酸时,发生反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com