
科目: 来源: 题型:
反应N2O4(g)2NO2(g);ΔH=+57 kJ·mol-1,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. 由状态B到状态A,可以用加热的方法
D. A、C两点气体的平均相对分子质量:A>C
查看答案和解析>>
科目: 来源: 题型:
2SO2(g)+O2(g) ![]() 2SO3(g)是制备硫酸的重要反应。下列叙述正确的
2SO3(g)是制备硫酸的重要反应。下列叙述正确的
A. 催化剂V2O5不改变该反应的逆反应速率
B. 增大容器体积,反应速率一定增大
C. 该反应是放热反应,降低温度将缩短反应达到平衡的时间
D. 在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为![]()
查看答案和解析>>
科目: 来源: 题型:
在室温下等体积的酸和碱的溶液,混合后pH一定等于7的是( )
A. pH=3的硝酸和pH=11的Ba(OH)2溶液 B. pH=3的盐酸和pH=11的氨水
C. pH=3的硫酸和pH=11的KOH D. pH=3的醋酸和pH=11的KOH溶液
查看答案和解析>>
科目: 来源: 题型:
I2在KI溶液中存在下列平衡:![]()
![]()
![]()
某I2、、KI混合溶液中,![]() 的物质的量浓度c(
的物质的量浓度c(![]() )与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
A. 反应 ![]()
![]()
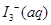 △H>0
△H>0
B.若温度为![]() ,反应的平衡常数分别为
,反应的平衡常数分别为![]()
C.若反应进行到状态D时,一定有![]()
D.状态A与状态B相比,状态A的c(I2)大
查看答案和解析>>
科目: 来源: 题型:
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是( )
A.1mol/L甲酸溶液的pH约为3
B.HCN易溶于水
C.10mL1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应
D.在相同条件下,HCN溶液的导电性比强酸溶液的
查看答案和解析>>
科目: 来源: 题型:
常温下,某溶液中由水电离出来的c(H+)=1.0×10-13mol·L-1,该溶液可能是( )
A.亚硫酸 B.浓硫酸 C.硝酸钠水溶液 D.氢氧化钠水溶液
查看答案和解析>>
科目: 来源: 题型:
在0.1mol•L-1的醋酸溶液中,要使溶液的pH增大,同时又使醋酸根离子浓度增大,可加入的试剂是( )
A.CH3COONa浓溶液 B.1mol•L-1氨水
C.1mol•L-1H2SO4 D.2 mol•L-1 CH3COOH
查看答案和解析>>
科目: 来源: 题型:
某温度下,向各1ml相同pH值的盐酸和醋酸溶液分别加水稀释,平衡时pH值随溶液体积变化的曲线如下图所示。据图判断正确的是
A.Ⅱ为盐酸稀释时pH值变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点Kw的数值比c点Kw的数值大
D.b点酸的总浓度小于a点酸的总浓度
查看答案和解析>>
科目: 来源: 题型:阅读理解
向草酸(H2C2O4)溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色总是先慢后快。对其原因,某研究性学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究:
实验(1):在两支试管中分别加入10mL等浓度的草酸溶液,在②号试管中加入少量硫酸锰固体。然后在两支试管中分别加入5滴0.1 mol·L-1的硫酸酸化高锰酸钾溶液。现象如下(表1)
|
| ①号试管 | ②号试管 |
| 加入药品 | 草酸溶液 硫酸酸化高锰酸钾溶液 | 草酸溶液 硫酸酸化高锰酸钾溶液 硫酸锰固体 |
| 实验现象(褪色时间) | 溶液褪色很慢(30s) | 溶液褪色很快(2s) |
实验(2):在两支试管中分别加入5 mL等浓度的草酸溶液,在②号试管中再滴加10滴稀硫酸,然后各加入5滴0.1mol·L-1的高锰酸钾溶液。现象如下(表2)
| 编号 | ①号试管 | ②号试管 |
| 褪色时间 现象 | 100 s | 90 s |
| 均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
实验(3):取3支试管分别加入5 mL等浓度草酸溶液,然后在①、②、③号试管中依次加入10滴、1 mL、2 mL稀硫酸溶液,各加入5滴0.1 mol·L-1的高锰酸钾溶液,然后置于温度为65℃的水浴中加热。观察现象(表3)。
| 编号 | ①号试管 | ②号试管 | ③号试管 |
| 褪色时间
实验现象 | 80 s | 100 s | 120 s |
| 均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
(1) 该研究性学习小组的实验目的是 。
(2)该研究性学习小组进行实验时所用的方法是科学实验中常用的一种方法,该方法叫 法;
(3)实验(1)得出的结论是 。
(4)由实验(2)和实验(3)得出的结论是(写三点)
_________________________,_____________________,_______________;
(5)据有关现象写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:
H2C2O4+ MnO4—+ = Mn2++ + H2O
查看答案和解析>>
科目: 来源: 题型:阅读理解
实验室常利用甲醛法(HCHO)测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH4+ +6HCHO =3H++6H2O+(CH2)6N4H+[滴定时,1 mol (CH2)6N4H+消耗NaOH与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500 g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤III 填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积________________(填“偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察____________
(A)滴定管内液面的变化 (B)锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由_________色变成_________色。
(2)滴定结果如下表所示:
| 滴定 次数 | 待测溶液的体积 /mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
滴定时消耗NaOH标准溶液的体积的平均值V=__________mL;若NaOH标准溶液的浓度为0.1010 mol·L-1,则250 mL溶液中的n(NH4+)=__________mol,该样品中氮的质量分数为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com