
科目: 来源: 题型:
在一种酸性溶液中可能存在Fe3+、NO3-、Cl-、I-中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推断溶液中
A.一定含有I-,不能确定是否含有Cl- B.可能含有NO3-、Cl-和I-
C.可能含有NO3- D.肯定含有Fe3+
查看答案和解析>>
科目: 来源: 题型:
质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为
A.大于2cmol/L B.等于2c mol/L
C.小于2cmol/L D.在c mol/L~2c mol/L之间
查看答案和解析>>
科目: 来源: 题型:
已知反应X +Y = M + N为吸热反应,对这个反应的下列说法中正确的是
A.X的能量一定低于M的,Y的能量一定低于N的
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.一定温度下,1L0.5mol·L-1NH4Cl溶液与1L0.25mol·L-1NH4Cl溶液中NH4+ 物质的量之比为2:1
B.100g硫酸溶液的物质的量浓度为18.4mol/L,用水稀释到物质的量浓度为9.8mol/L,需要水100g.
C.标准状况下,22.4LCH3Cl和CHCl3的混合物中所含有的碳原子个数一定为NA
D.在2Na2O2+2CO2=2Na2CO3+O2反应中,每生成16g氧气,则转移NA个电子
查看答案和解析>>
科目: 来源: 题型:
下列关于某溶液所含离子检验的方法和结论正确的是
A.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,说明有Ca2+
B.通入少量Cl2后,溶液变为黄色,再加入淀粉溶液后,溶液变蓝,说明有I-
C.加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中一定有CO32-或SO32-
D.往溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成,说明一定有SO42-
查看答案和解析>>
科目: 来源: 题型:
(共6分)瑞典皇家科学院宣布,将2007年诺贝尔化学奖授予德国马普学会弗里茨-哈伯(Fritz-Haber)研究所的格哈德·埃特尔(Gerhard Ertl)教授,以表彰他在固体表面化学过程研究领域作出的开拓性成就。合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为_________。
(2)当催化剂中Fe2+与Fe3+物质的量之比为1:2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为_________(用小数表示)。
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量碳粉,发生如下反应:
2Fe2O3 +C=4FeO +CO2↑,为制得这种催化活性最高的催化剂,应向480g Fe2O3粉末中加入碳粉的质量为_________ g。
查看答案和解析>>
科目: 来源: 题型:
(共14分) 2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响?(填“有影响”或“无影响”) 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(2)图中△H= KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
(4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= mol·L-1·min-1、υ(SO3)= mol·L-1·min-1;
(5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
查看答案和解析>>
科目: 来源: 题型:
(共10分) 某无色溶液,其中可能存在Na+、Ba2+、AlO2-、S2-、SO32-、SO42-。取该溶液进行有关实验,实验结果如下图所示。
请回答下列问题:
(1)沉淀甲的化学式为 ;
(2)由溶液甲生成沉淀乙的离子方程式为 _______________;
(3)沉淀丙中一定含有 (填化学式,下同),可能含有 ;
(4)综合上述信息,该溶液中肯定存在的离子有 ___________________。
查看答案和解析>>
科目: 来源: 题型:
(共10分)根据下面物质间转换的框图,回答有关问题:
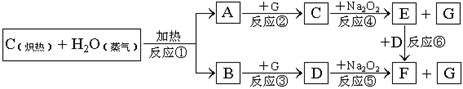
(1)由反应①产生的A、B混合物的工业名称是 。
(2)写出框图中D、E的化学式:D ;E
(3)如果2mol Na2O2与足量水蒸气反应,可得标准状况下气体的体积是多少 L,同时反应中转移电子总数是 。(NA表示阿佛加德罗常数)
(4)请设计一个简单易行的小实验,证明反应⑤是放热反应。实验方法是
(5)如果A、B混合气体7.8g(平均摩尔质量10g·mol-1),在与G充分反应后,通过足量Na2O2层,可使Na2O2增重 g,并得到O2 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com