
科目: 来源: 题型:
(6分)已知1 molCO气体完全燃烧生成CO2 气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量;1 molCH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1)若1 molCH4气体完全燃烧生成CO2气体和水蒸气,放出热量为 890 kJ(填“>”、 “<”、“= ”)。
(2)若将a molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水时,则放出热量(Q)的取值范围是 。
(3)若将a molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水,且CO2和水的物质的量相等时,则放出热量(Q)的取值范围是___________________________。
查看答案和解析>>
科目: 来源: 题型:
(9分)与甲醇燃料电池相比,乙醇燃料电池具有毒性低、理论能量密度高等优点,因此被广泛认为是更有前途的燃料电池。下图是一个乙醇燃料电池工作时的示意图。乙池中的两个电极均为石墨电极,乙池中盛有100 mL3.00 mol/L的CuSO4溶液。请回答下列问题:
(1) 在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出30kJ热量,表示该反应的热化学方程式为 。
(2)N的电极反应式为 。
(3)在此过程中,乙池中某一电极析出金属铜6.4g时,甲池中理论上消耗氧气 升
(标准状况下)
(4)在此过程中,若乙池中两电极产生的气体恰好相等时(假设标准状况下),理论上需通入乙醇 g?
查看答案和解析>>
科目: 来源: 题型:
(4分)下列有关实验操作中,正确的是
A.沾附在试管内壁上的油脂,用热碱液洗涤
B.除去苯中含有的苯酚 ,先加浓溴水再过滤。
C.检验卤代烃中的卤素原子,先将卤代烃与NaOH溶液共热,再加AgNO3溶液
D.除去乙酸乙酯中的乙酸, 加入氢氧化钠溶液。
E.检验淀粉的水解产物,先将淀粉与稀硫酸共热一段时间,然后加入氢氧化钠中和硫酸,再加入银氨溶液并水浴加热。
查看答案和解析>>
科目: 来源: 题型:
(13分)下面是甲、乙、丙三位同学制取乙酸乙酯的过程。
(1)甲、乙、丙三位同学均采取乙醇、冰醋酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸的作用是 ;
(2)甲、乙、丙三位同学分别设计了如图所示三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是 (选填“甲”或“乙”)。丙同学设计了丙装置,用球形干燥管代替玻璃管,除了起到冷凝作用外,另一重要作用是 。
(3)试管②中饱和Na2CO3的作用除了溶解乙醇、降低乙酸乙酯溶解度外,还可以 。
(4)从试管②中分离出乙酸乙酯的实验操作是 。
(5)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,
就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反
应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
查看答案和解析>>
科目: 来源: 题型:
为了建设环境友好型社会,节能减排将成为我国政府目前工作的重点,因此节约能源与建设新能源是摆在当前的一个课题。针对这一现象,某化学学习研究性小组提出如下方案,你认为不够科学合理的是
A.采用电解水法制取氢气作为新能源
B.加大开发太阳能、水能、风能、地热能等能源力度,减少化石燃料的使用
C.研制推广以乙醇为燃料的汽车
D.生产、生活中,努力实现资源的循环利用
查看答案和解析>>
科目: 来源: 题型:
反应2A(g) 2B(g)+E(g) △H>0, 达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是
A.加压 B.减压 C.减少E的浓度 D.降温
查看答案和解析>>
科目: 来源: 题型:
在2A+B=3C+4D反应中,表示该反应速率最快的数据是
A.υA =0.5mol·L-1·s-1 B.υB = 0.3mol·L-1·s-1
C.υC = 0.8mol·L-1·s-1 D.υD = 1.0mol·L-1·s-1
查看答案和解析>>
科目: 来源: 题型:
将纯水加热至较高温度,下列叙述正确的是
A.水的离子积变大、pH变小、呈酸性
B.水的离子积不变,pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性
D.水的离子积变大、pH变小、呈中性
查看答案和解析>>
科目: 来源: 题型:
如图表示中和滴定时某同学的一个操作,下列叙述正确的是
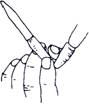
A.这是一个错误操作
B.该操作是为了排除滴定管内气泡
C.该操作是为了防止滴定管漏液
D.该操作是为了调节滴定管内液体的液面高低
查看答案和解析>>
科目: 来源: 题型:
已知:
①CH4 ( g )+4NO2( g)=4NO( g ) +CO2( g )+2H2O( g ) △H=一574 kJ·mol-1
②CH4 ( g )+4NO( g )=2N2(g )+CO2( g )+2H2O( g) △H=一1160 kJ·mol一1
下列正确的选项是
A.CH4 ( g )+2NO2( g )= N2( g )+CO2 ( g )+2H2O( l) △H=一867 kJ·mol-1
B.CH4 ( g )+2NO2( g )= N2( g )+CO2 ( g )+2H2O( g) △H=一867 kJ·mol-1
C.CH4 ( g )+2NO2( g )= N2( g )+CO2 ( g )+2H2O( g) △H=一586kJ·mol-1
D.CH4 ( g)+2NO2 ( g )= N2( g )+CO2 ( g)+2H2O ( g) △H=+586kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com