
科目: 来源: 题型:单选题
| 序号 | 实验方案 | 现象、结论 |
| A | 加入盐酸 | 产生无色气体,含铝、铁、镁三种元素 |
| B | 加入NaOH 溶液 | 有无色气体产生,含有铝元素 |
| C | 加入盐酸后,所得溶液中再加入少量NaOH溶液 | 产生白色沉淀,含有镁元素 |
| D | 加入KSCN 溶液 | 溶液呈血红色,含有铁元素 |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
 实验室要配制0.5mol/L的NaOH溶液100mL,则:
实验室要配制0.5mol/L的NaOH溶液100mL,则:查看答案和解析>>
科目: 来源: 题型:单选题
 Na2SiO3
Na2SiO3 H2SiO3
H2SiO3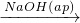 NaAlO2
NaAlO2 Al(OH)3
Al(OH)3 Fe2O3
Fe2O3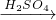 Fe2(SO4)2
Fe2(SO4)2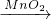 Cl2
Cl2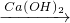 Ca(ClO)2
Ca(ClO)2查看答案和解析>>
科目: 来源: 题型:解答题
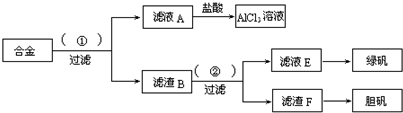
查看答案和解析>>
科目: 来源: 题型:解答题
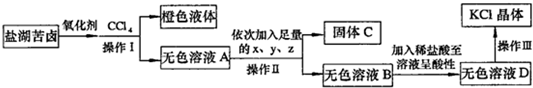
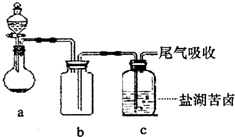
查看答案和解析>>
科目: 来源: 题型:单选题
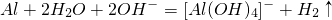
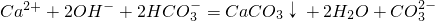
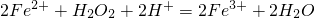
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
 ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(ρ=1.84g?cm-3)110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质.
ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(ρ=1.84g?cm-3)110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质.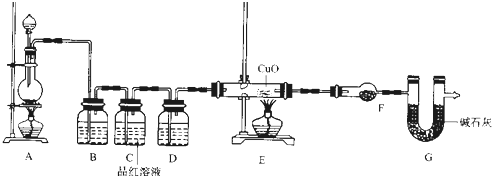
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com