
科目: 来源: 题型:
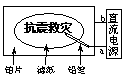
某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是:
A.铅笔端作阳极,发生还原反应 B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生 D.a点是负极,b点是正极
查看答案和解析>>
科目: 来源: 题型:
竖炉冶铁工艺流程如图,使天然气产生部分氧化,并在特殊的燃烧器中使氧气和天然气燃烧CH4(g)+2O2(g)=CO2(g)+2H2O(g),催化反应室发生的反应为:CH4(g)+H2O(g) CO(g)+3H2(g) ∆H1=+216kJ/mol;CH4(g)+ CO2(g)
2CO(g) + 2H2(g) ∆H2=+260kJ/mol(不考虑其他平衡的存在),下列说法正确的是
A.增大催化反应室的压强,甲烷的转化率减小
B.催化室需维持在550~750℃,目的仅是提高CH4转化的速率
C.设置燃烧室的主要目的是产生CO2和水蒸气作原料气与甲烷反应
D.若催化反应室中,达到平衡时,容器中n(CH4)=amol/L,n(CO)=bmol/L
n(H2)=cmol/L,则通入催化反应室的CH4的物质的量为a+(b+c)/4
查看答案和解析>>
科目: 来源: 题型:
21、(4分)某同学设计用AlCl3溶液和Na2S溶液反应制取硫化铝(Al2S3)固体,你认为他能达到目的吗? 原因是(用离子方程式表示): 。配制Na2S溶液时,为了防止水解,常向溶液中加入少量 ,用离子方程式表示Na2S的水解 。
查看答案和解析>>
科目: 来源: 题型:
(4分)由金红石(TiO2)制取单质Ti,涉及到的步骤为:
![]()
已知:①![]()
②![]()
③![]()
则(1) 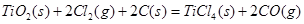 的
的![]() =________________。
=________________。
(2) 碳在氧气中不完全燃烧生成CO的热化学方程式为__________________________。
查看答案和解析>>
科目: 来源: 题型:
(2分)一定量的盐酸和过量的锌粒反应产生氢气,为了减慢反应速率,又不影响产生的氢气的总量,下列措施可行的是 ①加入NaOH固体②加入一定量的水③加入少量硫酸钠溶液④加入少量硫酸铜溶液⑤加入CH3COONa固体⑥加入KNO3溶液。
查看答案和解析>>
科目: 来源: 题型:
(5分)甲、乙两同学拟用实验确定某酸HA是弱电解质。他们的方案分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,说明HA是弱电质的理由是测得溶液的pH___1(选填>,<,=)。简要说明pH试纸的使用方法:
(3) 乙方案中,说明HA是弱电解质的现象是_________ 。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
查看答案和解析>>
科目: 来源: 题型:
(8分)水的电离平衡曲线如图所示。
(1)若以A点表示25℃时水的电离平衡的离子浓度,当温度升高到100℃时,水的电离平衡状态移动到B点,则此时水的离子积从 变化到 。(2)将PH=8的Ba(OH)2溶液与PH=5的稀盐酸混合,并保持100℃的恒温,致使混合溶液的PH=7,则Ba(OH)2和盐酸的体积之比为 。
(3)已知的离子积为
若某温度下
的溶解度为0.74g,设饱和溶液的密度为
,其离子积约为 。
(4)已知25℃时,0.1 L 0.1 mol·L-1的NaA溶液的pH = 10,则NaA溶液中所存在的离子的物质的量浓度由大到小的顺序为 。
查看答案和解析>>
科目: 来源: 题型:
(6分)请用学过的知识分析其中的化学原理并写出化学方程式,属于离子反应的请写出离子方程式。(1)将氯气通入熟石灰即可制的漂白粉【漂白粉的有效成分是次氯酸钙Ca(ClO)2,商品漂白粉往往含有Ca(OH)2等杂质】 。(2)漂白粉之所以具有漂白作用是由于Ca(ClO)2在水溶液中发生水解反应生成具有强氧化性的物质 。(3)Ca(OH)2杂质的存在使溶液的碱性增强,因此漂白作用进行缓慢。要在短时间受到漂白效果,必须除去Ca(OH)2,所以工业上使用漂白粉是常加入少量弱酸如醋酸等,或加入少量的稀盐酸 、
。(4)家庭使用漂白粉不必加酸,因为水中的CO2也起到了弱酸的作用 。(5)不要将漂白粉与洁厕剂等强酸性物质混合使用,因为在强酸性条件下二者可以发生氧化还原反应生成一种有毒气体:
查看答案和解析>>
科目: 来源: 题型:
(7分)电解原理在化学工业中广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和CuSO4溶液,实验开始时,同时在两边各滴入石蕊试液,则①Y电极上的电极反应式为
②在Y电极附近观察到的现象是
(2)若X、Y都是铜电极,a是浓度均为2mol·L-1的AgNO3与Cu(NO3)2的混合溶液1L,电解一段时间后X电极上有12.8g铜析出,此时直流电源已输出 mol电子。
(3)用石墨电极电解100mLH2SO4和CuSO4混合液,通电一段时间后,两极各出现气体3.36L(标准状况),求原来溶液中CuSO4的浓度 。
查看答案和解析>>
科目: 来源: 题型:
(4分)吸热反应N2(g)+O2 (g) ![]() 2NO(g),在2000℃时,K=6.2×10-4.2000℃时,在10L密闭容器内放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2,通过计算回答:(1)此反应的初始状态是否为化学平衡状态?
2NO(g),在2000℃时,K=6.2×10-4.2000℃时,在10L密闭容器内放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2,通过计算回答:(1)此反应的初始状态是否为化学平衡状态?
(2)若非化学平衡状态,反应将向哪个方向进行?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com