
科目: 来源: 题型:
某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如右图所示。据图判断正确的是 ( )
 A.Ⅱ为盐酸稀释时pH变化曲线
A.Ⅱ为盐酸稀释时pH变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点![]() 的数值比c点
的数值比c点![]() 的数值大
的数值大
D.b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
科目: 来源: 题型:
下列有关物质检验的实验结论正确的是 ( )
选项 实 验 操 作及 现 象 实 验 结 论
A 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 该溶液中一定含有![]()
B 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 该溶液中一定含有Fe2+
C 将某气体通入品红溶液中,品红溶液褪色 该气体一定是![]()
D NH3的水溶液可以导电 NH3是电解质
查看答案和解析>>
科目: 来源: 题型:
设NA代表阿伏加德罗常数(NA)的数值,下列说法正确的是 ( )
A.1 mol 硫酸钾中阴离子所带电荷数为NA
B.乙烯(C2H4 )和氮气组成的28g混合气体中含有NA 个原子
C.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA
D.将1mol氯化铁溶于1L水中,所得溶液含有NA个![]()
查看答案和解析>>
科目: 来源: 题型:
能用共价键键能的大小来解释的是 ( )
A.通常情况下,Br2呈液态,碘呈固态 B.CH4分子是正四面体结构
C.惰性气体一般难发生化学反应 D.N2的化学性质比O2稳定
查看答案和解析>>
科目: 来源: 题型:
法国里昂的科学家最近发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是 ( )
A.该粒子不显电性 B.该粒子质量数为4
C.在周期表中与氢元素占同一位置 D.该粒子质量比氢原子大
查看答案和解析>>
科目: 来源: 题型:
为预防H1N1甲型流感,每天用“84”消毒液(NaClO溶液)消毒,下列说法正确的是( )A.NaClO溶液的消毒原理是使蛋白质变性
B.1molCl2与足量NaOH溶液反应转移2mol电子
C.NaClO溶液的漂白原理与Na2O2、SO2相同
D.“84”消毒液与“洁厕灵”(盐酸)共同使用,可达到既清洁又消毒的双重效果
查看答案和解析>>
科目: 来源: 题型:
广州2010年承办第16届亚运会。下列措施有利于节能减排、改善环境质量的是( )
①在大亚湾核电站已安全运行多年的基础上,广东将继续发展核电,以减少火力发电带来的二氧化硫和二氧化碳排放问题
②积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料
③加速建设地铁等轨道交通,促进珠三角城市一体化发展,减少汽车尾气排放
④发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾
A.①②③④ B.①②⑤ C.①②④⑤ D.③④⑤
查看答案和解析>>
科目: 来源: 题型:阅读理解
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选择其中一题作答。若两题都做,则按A题评分。
A.CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:
①CuCl可以由CuCl2用适当的还原剂如S02、SnCl2等还原制得:
![]()
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:
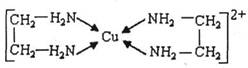
请回答下列问题:
(1)基态Cu原子的核外电子排布式为_________。H、N、O三种元素的电负性由大到小的顺序是_____。
(2)SO2分子的空间构型为____________。与SnCl4互为等电子体的一种离子的化学式为_________。
(3)乙二胺分子中氮原子轨道的杂化类型为_____________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_____________________________________________。
 (4)②中所形成的配离子中含有的化学键类型有__________。(填字母)
(4)②中所形成的配离子中含有的化学键类型有__________。(填字母)
a.配位键 b.极性键 c.离子键 d.非极性键
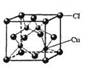
(5)CuCl的晶胞结构如右图所示,其中Cl原子的配位数为_________。
B.阿司匹林(乙酰水杨酸)是常用的解热镇痛药,以下是合成阿司匹林的工艺流程。
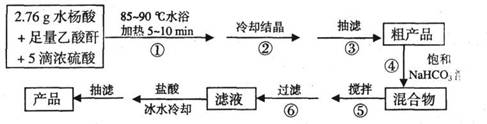
已知:①反应方程式为
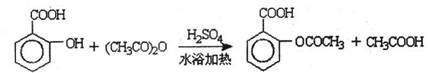
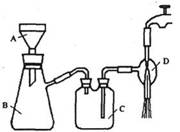
②抽滤的实验装置如右图所示。
请回答有关问题:
(1)仪器A的名称是_____________。
(2)在步骤②中,若冷却结晶时未出现结晶,可以___________,
促使晶体析出。
(3)实验时,当仪器B中液面高度快达到支管口位置时,应进行
的操作是____________________________________________。
(4)仪器C中两玻璃导管的位置是否正确?答:_________。(填“正确”或“不正确”)
(5)在步骤④中,用饱和NaHC03溶液可以将阿司匹林和剐产物等分离,其化学原理是
_________________________________________。要检测产品中是否含有水杨酸,其实验操作是_____________________________________________________。
(6)在步骤⑤中,搅拌使反应充分进行至_____________为止。
(7)若实验得到2.70g纯净的阿司匹林,则产品的产率为____________。
查看答案和解析>>
科目: 来源: 题型:
草酸(H2C204)是一种重要的化工原料。已知常温下0.01 mol·L-l的H2C204、KHC204、K2C204溶液的pH如下表所示。 。.
|
| H2C204 | KHC204 | K2C204 |
| pH | 2.0 | 3.1 | 8.1 、 |
(1)在其它条件不变时,下列措施能使KHC204溶液中c(K+):c(HC204-)接近1:1的是_________(填字母)。
A.加入适量的H2C204 B.加入适量的KHC204
C.加入适量的Na2C204 D.升高溶液的温度
(2)取一定质量H2C204·2H20和KHC204的混合物,加水溶解,配成250 mL溶液,取两份此溶液各25 mL,向第一份溶液中先加入几滴酚酞试液,再滴加0.25 mol·L-l NaOH溶液至20.00 mL时,溶液由无色变为浅红色;向第二份溶液中滴加适量3 mol·L-l H2S04溶液酸化后,用0.10 mol·L-l KMnO4溶液滴定,当消耗KMnO4溶液16.00 mL时,溶液由无色变为浅紫红色。请回答下列问题:
①完成离子方程式:5C2042-+2Mn04-+16H+=10______+2Mn2++8H2O。
②原混合物中H2C204·2H20和KHC204的物质的量之比为__________。
(3)某实验小组用如图所示的装置探究FeC204·2H20在隔绝空气条件下受热分解的产物。当36.0g FeC204·2H20充分反应后,残留固体质量为13.6g,浓硫酸增重7.2g,碱石灰增重11.0g。求残留固体的成分和物质的量。(已知FeC204·2H20的相对分子质量为180;设反应产生的气体被充分吸收)
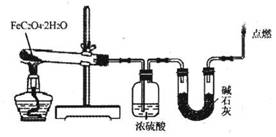
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com