
科目: 来源: 题型:
下列说法中,正确的是
A. 在化学反应中,发生物质变化的同时不一定发生能量变化
B. 催化剂能改变化学反应的平衡转化率
C. △H的大小与热化学方程式中物质的系数无关
D. 反应产物的总能量大于反应物的总能量时,△H>0
查看答案和解析>>
科目: 来源: 题型:
有机物A可以通过不同的反应得到下列物质:

(1)A的结构简式是 _________
(2)写出由A制取B的化学方程式: ________________________
(3)写出A制取E两种物质的有机反应类型: _______________;
A与 ____________(填写化学式)反应生成D。
(4)有机物C中共面的碳原子最多是_____个。
(5)芳香族化合物F是A的同分异构体,1molF可以和3mol NaOH发生中和反应;F苯环上的一氯代物只有一种。写出F两种可能的结构简式 ______________________。
查看答案和解析>>
科目: 来源: 题型:
现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH—、C1—、CO32—、NO3—、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)写出D为_________________
(2)将C溶液逐滴加入等体积、等物质量的浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为:_____________________。
(3)写出E溶液与过量的B溶液反应的离子方程式____________________________________。
(4)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H=-aKJ·mol-1。请写出B与C的稀溶液反应的热化学方程式___________________________________________________。
(5)在100mL0.1mol·L-1E溶液中,逐滴加入35mL2mol·L-1NaOH溶液,最终得到沉淀物质的量为_____。
查看答案和解析>>
科目: 来源: 题型:
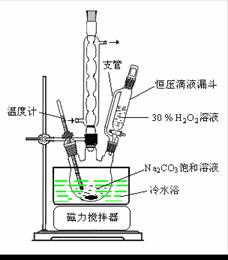
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
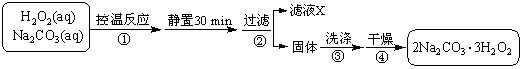 已知:主反应 2Na2CO3 (aq) + 3H2O2 (aq)
已知:主反应 2Na2CO3 (aq) + 3H2O2 (aq) ![]() 2Na2CO3·3H2O2 (s) ΔH < 0
2Na2CO3·3H2O2 (s) ΔH < 0
副反应 2H2O2 = 2H2O + O2↑
滴定反应 6KMnO4 + 5(2Na2CO3·3H2O2) +19H2SO4 =
3K2SO4 + 6MnSO4 +10Na2SO4 + 10CO2 ↑ + 15O2↑ + 34H2O
 50 °C时 2Na2CO3·3H2O2 (s) 开始分解
50 °C时 2Na2CO3·3H2O2 (s) 开始分解
请回答下列问题:
(1)图中支管的作用是 。
(2)步骤①的关键是控制温度,其措施有 、
和 。
(3)在滤液X中加入适量NaCl固体或无水乙醇,
均可析出过碳酸钠,原因是 。
(4)步骤③中选用无水乙醇洗涤产品的目的
是 。
(5)下列物质中,会引起过碳酸钠分解的有 。
A.Fe2O3 B.CuO
C.Na2SiO3 D.MgSO4
(6)准确称取0.2000 g 过碳酸钠于250 mL 锥形瓶中,加50 mL 蒸馏水溶解,再加50 mL 2.0 mol·L-1 H2SO4,用2.000×10-2 mol·L-1 KMnO4 标准溶液滴定至终点时消耗30.00 mL,则产品中H2O2的质量分数为 。
查看答案和解析>>
科目: 来源: 题型:
U、V、W、X、Y为短周期元素,且原子半径依次增大,U、V同主族,V、W、X、Y处于同周期,U的最高价氧化物所对应的水化物与其气态氢化物反应生成盐A,U、W、Y的最高价氧化物对应的水化物能互相反应生成盐,Z为血红蛋白中所必需的金属元素,且U、W、Z分别能与氧元素形成U203、W2O3、Z2O3。
回答下列问题:
(1)U的气态氢化物分子的电子式为____________________,盐A中阳离子的检验方法是_________________________;
(2) 元素V、W、X、Y的第一电离能的大小关系是:______________________,Z原子的最外层电子排布式__________;
(3)W的单质与Y的最高价氧化物对应的水化物的溶液反应,其离子方程式是_________;
(4)z单质与水在一定条件下反应的化学方程式为________________________;
(5)已知:Z(s)+1/2O2(g)=ZO(s) ![]()
W(s)+3/2O2(g)= W2O3(s) ![]()
W的单质和ZO反应的热化学方程式是______________________________________。
查看答案和解析>>
科目: 来源: 题型:
将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.9mol,这些气体恰好能被500ml 2mol/LNaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量为( )
A.0.2mol B.0.4mol C.0.8mol D.0.9mol
查看答案和解析>>
科目: 来源: 题型:
已知铅+2价稳定,6种物质:H2O、PbO2、Pb(NO3)2、HMnO4、HNO3和Mn(NO3)2可以组成一个化学方程式。下列有关说法正确的是( )
A.反应物中发生氧化反应的物质PbO2
B.被还原的元素是Mn(NO3)2中Mn
C.反应中1mol氧化剂得到5mol电子。
D.请将反应物配平后的PbO2与Mn(NO3)2系数之比5:2
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.按系统命名法, 的名称为2,5,6-三甲基-4-乙基庚烷
的名称为2,5,6-三甲基-4-乙基庚烷
B.常压下,正戊烷、异戊烷、新戊烷的沸点依次增大
C.肌醇 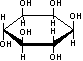 与葡萄糖
与葡萄糖 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物
的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物
D.1.0 mol的  最多能与含5.0 mol
最多能与含5.0 mol
NaOH的水溶液完全反应
查看答案和解析>>
科目: 来源: 题型:
已知电极上每通过96 500 C的电量就会有1 mol电子发生转移。精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量。实际测量中,常用银电量计,如图所示。下列说法不正确的是( )

A.电量计中的银棒应与电源的正极相连,铂坩埚上发生的电极反应是:Ag+ + e- = Ag
B.称量电解前后铂坩埚的质量变化,得金属银的沉积量为108.0 mg,则电解过程中通过电解池的电量为96.5 C
C.实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋。若没有收集网袋,测量结果会偏高。
D.若要测定电解饱和食盐水时通过的电量,可将该银电量计中的银棒与待测电解池的阳极相连,铂坩埚与电源的负极相连。
查看答案和解析>>
科目: 来源: 题型:
下图是铝热反应(2Al+Fe2O3Al2O3 +2Fe)的实验装置,有关该反应的下列说法中正确的是( )
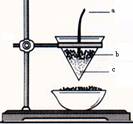
A.a 为镁条
B.b为氧化铁与铝粉混合物
C.2mol氧化剂参与反应则电子转移6NA个电子
D.还原剂与氧化产物的物质的量之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com