
科目: 来源: 题型:
关于氢键,下列说法正确的是
A、某些含氢元素的化合物中一定有氢键
B、氢键比分子间作用力强,所以它属于化学键
C、DNA中的碱基互补配对是通过氢键来实现的
D、H2O是一种非常稳定的化合物,这是由于氢键所致
查看答案和解析>>
科目: 来源: 题型:
当镁原子由1s22s22p63s2 →1s22s22p63p2时,以下认识正确的是
A、镁原子由基态转化成激发态,这一过程中吸收能量
B、镁原子由激发态转化成基态,这一过程中释放能量
C、转化后位于p能级上的两个电子处于同一轨道,且自旋方向相同
D、转化后镁原子与硅原子电子层结构相同,化学性质相似
查看答案和解析>>
科目: 来源: 题型:
多数晶体中的微观微粒服从紧密堆积原理的根本原因是( )
A、便于形成规则的几何外形
B、微观微粒结合得越紧密,体系总能量越低,体系越稳定
C、便于使晶体具有对称性
D、为了使晶体具备各向异性
查看答案和解析>>
科目: 来源: 题型:
构造原理揭示的电子排布能级顺序,实质是各能级能量高低顺序、若以E表示某能级的能量,下列能量大小顺序中正确的是
A、E(3s)>E(3p)>E(3d) B、E(3s)>E(2s)>E(1s)
C、E(4f)>E(4s)>E(3d) D、E(5s)>E(4s)>E(4f)
查看答案和解析>>
科目: 来源: 题型:
现有四种元素的基态原子的电子排布式如下:① [Ne]3s23p4; ②1s22s22p63s23p![]() 3;③1s22s22p5。则下列有关比较中正确的是( )
3;③1s22s22p5。则下列有关比较中正确的是( )
A、最高正化合价:③>②>① B、原子半径:③>②>①
C、电负性:③>②>① D、第一电离能:③>②>①
查看答案和解析>>
科目: 来源: 题型:
下列关于化学键的说法中正确的是( )
A、金属键可以看做是![]() 许多原子共用许多电子所形成
许多原子共用许多电子所形成![]() 的强烈相互作用,所以和共价键类似,也有饱和性和方向性
的强烈相互作用,所以和共价键类似,也有饱和性和方向性
B、配位键常用A→B表示,其中A原子可以提供接受孤电子对的空轨道
C、含有π键的分子在反应时,π键是化学反应的积极参与者
D、![]() 所有配合物都存在配位键,所有含配位键化合物都是配合物
所有配合物都存在配位键,所有含配位键化合物都是配合物
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,正确的是( )
A、1s电子云界面图是一个球面,表示在这个球面以外,电子出现的概率为零
B、σ键是镜面对称,而π键是轴对称
C、在能层、能级、以及电子云的伸展方向确定时,电子的运动状态才能确定下来
D、在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析
查看答案和解析>>
科目: 来源: 题型:
㈠2SO2(g)+O2(g) ![]() 2SO3(g)反应过程的能量变化如图
2SO3(g)反应过程的能量变化如图 所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.
所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.
请回答下列问题:
⑴图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
⑵图中△H= KJ·mol-1;
⑶已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求写出计算过程)。
 ㈡进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,表中是部分化学键的键能数据:
㈡进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,表中是部分化学键的键能数据:
| 化学键 | P—P | P—O | O==O | P==O |
| 键能/kJ·mol-1 | 197 | 360 | 499 | x |
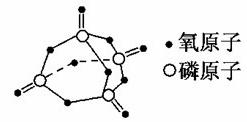
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图Ⅲ所示,则上表中x=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com