
科目: 来源: 题型:
体积一定的绝热密闭容器中加入等物质的量的X、Y,进行如下可逆反应:
X(g)+Y(g)![]() Z(g)+W(s)ΔH>0下列叙述正确的是
Z(g)+W(s)ΔH>0下列叙述正确的是
A.若继续充入X,平衡向正反应方向移动,Y的转化率增大
B.若继续充入Z,平衡逆向移动,Z的体积分数减小
C.若移走部分W,平衡正向移动
D.平衡后移走X,上述反应的ΔH减小
查看答案和解析>>
科目: 来源: 题型:
下图是198 K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是
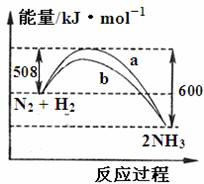
A.该反应的热化学方程式为:N2 + 3H2![]() 2NH3 △H =-92 kJ·mol-1
2NH3 △H =-92 kJ·mol-1
B.向一密闭容器中加入1 molN2和3 molH2充分反应后,放出92 kJ热量
C.b曲线可能是加入催化剂时的能量变化曲线
D.加入正催化剂可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目: 来源: 题型:
已知化学反应:①C(s)+1/2O2(g) = CO(g) △H1<0
②CO(g) +1/2O2(g) = CO2(g) △H2<0
③C(s)+O2(g) = CO2(g) △H3<0;
下列说法正确的是(相同条件下)
A.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量
B.反应②反应物的键能之和大于产物键能之和
C.△H1+△H2>△H3
D.△H3 >△H1 ,故CO2比CO稳定
查看答案和解析>>
科目: 来源: 题型:
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
已知:①Sn(s,白)+2HCl(aq)= SnCl2(aq)+H2(g) ΔH1
②Sn(s,灰)+2HCl(aq)= SnCl2(aq)+H2(g) ΔH2
③Sn(s,灰)![]() Sn(s,白) ΔH3 = +2.1 kJ·mol-1
Sn(s,白) ΔH3 = +2.1 kJ·mol-1
下列说法正确的是
A.ΔH1>ΔH2
B.灰锡和白锡本质上是同一种物质
C.相同条件下,白锡越多,与盐酸反应越快
D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏
查看答案和解析>>
科目: 来源: 题型:
下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热
ΔH=2×(-57.3) kJ•mol-1
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+566.0 kJ•mol-1
C.需要加热才能发生的反应一定是吸热反应
D.Ba(OH)2·8H2O与NH4Cl反应的焓变小于0,所以在常温下能自发进行
查看答案和解析>>
科目: 来源: 题型:
化学与生活、社会密切相关。下列说法不正确的是
A.乙醇是一种再生能源,充分燃烧的产物不污染环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
查看答案和解析>>
科目: 来源: 题型:
(1)过氧化钠可用于作制氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(2)在标准状况下,33.6 L氯气与红热的铁丝完全反应,反应的化学方程式为 ,最多可消耗铁的物质的量为 mol。
查看答案和解析>>
科目: 来源: 题型:
实验室要配制1 mol·L-1的稀硫酸250mL,回答下列问题:
(1)需要98%密度为1.84g/cm3的浓硫酸 mL
(2)配制时,该实验两次用到玻璃棒,其作用分别是 、 。
(3)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不影响”)
①没有洗涤烧杯和玻璃棒。 。
②如果加水超过了刻度线,取出水使液面恰好到刻度线。 。
③容量瓶没有干燥。
④定容时俯视容量瓶瓶颈刻度线
查看答案和解析>>
科目: 来源: 题型:
甲乙两人分别用不同的方法配制100ml 3.6mol/L的稀硫酸。
(1)甲:量取20 ml 18 mol/L浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 ml 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
① 实验所用的玻璃仪器除烧杯和容量瓶外,还有 ;
② 将溶液转移到容量瓶中的正确操作是
;
③ 定容的正确操作是
。
(2)乙:用100 ml 量筒量取20 ml 浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 ml 刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中错误之处
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com