
科目: 来源: 题型:
下列说法正确的是
A.元素的单质可由氧化或还原含该元素的化合物来制得
B.反应中失去电子越多的金属单质,其还原性就越强
C.阳离子只能得到电子被还原,只能作氧化剂
D.有单质参加的反应一定是氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
某实验小组只领取下列仪器或用品:铁架台、铁圈、三角架、石棉网、烧杯、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、蒸馏烧瓶、温度计、冷凝管、尾接管、锥形瓶、火柴、滤纸。只应用上述仪器或用品,不能进行的实验操作是
A.蒸发 B.萃取 C.过滤 D.蒸馏
查看答案和解析>>
科目: 来源: 题型:
下列实验操作中错误的是
A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C.蒸发结晶时应将溶液蒸干后停止加热D.可以用四氯化碳萃取碘水中的碘单质
查看答案和解析>>
科目: 来源: 题型:
下列有关胶体的叙述中不正确的是
A.淀粉溶胶中混有的氯化钠可以利用渗析的方法除去
B.向氢氧化铁胶体中逐滴滴入硫酸溶液,可以观察到先出现红褐色沉淀而后沉淀溶解形成澄清溶液
C.胶体介稳的主要原因是胶体带有电荷D.可以利用丁达尔效应来鉴别胶体和溶液
查看答案和解析>>
科目: 来源: 题型:
下列现象或应用不能用胶体知识解释的是
A.在河流入海口处易形成三角沙洲
B.用明矾净化饮用水
C.在氯化铁溶液中滴加氢氧化钠溶液出现红褐色沉淀
D.用石膏或卤水点制豆腐
查看答案和解析>>
科目: 来源: 题型:
下列关于混合物、纯净物、非电解质、强电解质和弱电解质的正确组合是
| 混合物 | 纯净物 | 非电解质 | 强电解质 | 弱电解质 | |
| A | 自来水 | 纯净的空气 | 甲烷 | 硝酸 | 碳酸 |
| B | 白酒 | 水银 | 一氧化碳 | 氯化银 | 磷酸 |
| C | 粗盐 | 冰 | 氨气 | 苛性钠 | 碳酸钙 |
| D | 爆鸣气 | 醋酸 | 氧气 | 硫酸钡 | 一水合氨 |
查看答案和解析>>
科目: 来源: 题型:
Ⅰ、在10℃和4×105Pa的条件下,当反应aA(g) ![]() dD(g) + eE(g)建立平衡后,维持温度不变,逐步增大体系的压强,在不同压强下该反应建立平衡后,物质D的浓度见下表(在增大压强的过程中无其它副反应发生):
dD(g) + eE(g)建立平衡后,维持温度不变,逐步增大体系的压强,在不同压强下该反应建立平衡后,物质D的浓度见下表(在增大压强的过程中无其它副反应发生):
| 压强(Pa) | 4×105 | 6×105 | 1×106 | 2×106 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
①压强从4×105 Pa增加到6×105 Pa时平衡应向 反应方向移动(填“正”或 “逆”,下同),理由是
。
②压强从1×106 Pa 增加到2×106 Pa时,平衡向 反应方向移动。此时平衡向该方向移动的两个必要条件是 ; 。
Ⅱ、在10℃和1.01×105Pa的条件下,往容积可变的密闭容器中充入a molA和b molB,当反应2A(g)+ B(g) ![]() D(g) + E(s)建立平衡后,气体密度不变,已知各物质的摩尔质量(单位:g·mol-1)分别为A18、B46、D42、E40,则a:b为 。
D(g) + E(s)建立平衡后,气体密度不变,已知各物质的摩尔质量(单位:g·mol-1)分别为A18、B46、D42、E40,则a:b为 。
Ⅲ、已知T℃、P kPa时,往容积可变的密闭容器中充入2 mol X和1 mol Y,此时容积为V L。保持恒温恒压,使反应:2X(g)+Y(g)![]() 2Z(g)达到平衡时,Z的体积分数为0.4。若控制温度仍为T℃,另选一容积为V L的固定不变的密闭容器,往其中充入一定量的X和Y,使反应达到平衡,这时Z的体积分数仍为0.4。则充入的X和Y的物质的量应满足的关系是:a n(Y)<n(X)<b n(Y),则 a为 。
2Z(g)达到平衡时,Z的体积分数为0.4。若控制温度仍为T℃,另选一容积为V L的固定不变的密闭容器,往其中充入一定量的X和Y,使反应达到平衡,这时Z的体积分数仍为0.4。则充入的X和Y的物质的量应满足的关系是:a n(Y)<n(X)<b n(Y),则 a为 。
查看答案和解析>>
科目: 来源: 题型:
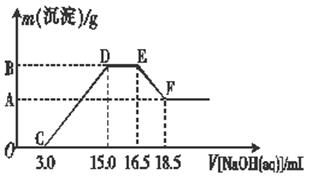
硝酸跟金属反应时,随着硝酸浓度的下降和金属活动性的增大,产物中氮元素的化合价会逐渐下降,它们可能是NO2、NO、N2O、N2或NH4NO3中的一种或几种。现有一定量的铁粉和铝粉组成的混合物跟100 mL稀硝酸充分反应,反应过程中无任何气体放出,往反应后的澄清溶液中逐渐加入4.00 mol·L-1的NaOH溶液,加入NaOH溶液的体积与产生沉淀的质量的关系如图所示(必要时可加热,忽略气体在水中的溶解):
请回答下列问题:
1)由图可知,往反应后的澄清溶液中加入NaOH溶液没有立即出现沉淀,其原因是__________________。
2)混合物跟稀硝酸充分反应后的产物中铁元素的化合价是 。
3)写出图中D―→E阶段所发生的反应的离子方程式: 。
4)纵坐标中A点的数值是 ,原稀硝酸的浓度是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com