
科目: 来源: 题型:
设NA表示阿伏伽德罗常数,下列叙述中不正确的是
①1mol NO2气体降温后颜色变浅,其所含的分子数仍然为NA
②标准状况下,含NA个氩原子的氩气体积约为22.4 L
③7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA
④1.0 L 0.1 mol/L的醋酸钠溶液中含CH3COOH、CH3COO-粒子总数为0.1NA
⑤Fe与0.1 mol氯气反应时失去的电子数为0.3 NA
⑥1 mol Cl2发生氧气还原反应时,转移的电子数一定是2 NA
A.①④⑥ B.②③⑤ C.①③⑤⑥ D.②④⑤
查看答案和解析>>
科目: 来源: 题型:
下列叙述中正确的是
①标准状况下,1L HCl和1L H2O的物质的量相同;②标准状况下,1g H2和14g N2的体积相同;③28g CO的体积为22.4L;④两种物质的物质的量相同,则它们在标准状况下的体积也相同;⑤在同温同体积时,气体物质的物质的量越大,则压强越大;⑥同温同压下,气体的密度与气体的相对分子质量成正比。
A.仅①②③ B.仅②⑤⑥ C.仅②③⑥ D.仅④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
下列是某同学自己总结的一些规律,其中正确的是
A.有些化学反应不属于化合反应、分解反应、置换反应、复分解反应中的任何一种反应
B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C.含有碳元素的化合物都属于有机化合物
D.一种氧化物不是酸性氧化物就一定是碱性氧化物
查看答案和解析>>
科目: 来源: 题型:
分类是化学学习与研究的常用方法,下列分类正确的是
A.Na2O、MgO、Na2O2均属于碱性氧化物
B.纯碱、烧碱、熟石灰均属于碱
C.酸、碱、盐之间发生的反应一定属于复分解反应
D.混合物、分散系、胶体从属关系如右图所示

查看答案和解析>>
科目: 来源: 题型:
下图是工业生产硝酸铵的流程。
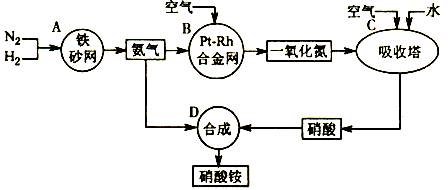
(1) 实验室制氨气的化学方程式为 ,
写出氨气转化为NO的化学方程式 。
(2) 在整个生产流程中两次通入空气的目的是
。
(3) A、B、C、D四个反应容器中的反应,属于氧化还原反应的是 (填反应容器字母代号),在NO2与水的反应中,氧化剂与还原剂的物质的量之比为 。
(4) 假设由NH3制NO的产率为100%,由NO制硝酸的产率为100%,然后利用制得的HNO3与剩余的NH3反应制备NH4NO3,则制硝酸用去的NH3占NH3总量的 %。
查看答案和解析>>
科目: 来源: 题型:
某课外小组利用下图装置在实验室制取SO2并探究其有关性质:

根据上图回答下列问题:
(1) 装置A中存在一处错误,改正这处错误 。
(2) 写出装置A中发生反应的化学方程式 ,
B瓶起的作用为 。
(3) 为了探究亚硫酸的酸性比碳酸酸性强的性质,有同学甲在装置B的出气口先连接装置II,再连接装置I,然后连接装置III。装置I的作用是 ,装置III中出现的实验现象为 。
(4) 同学乙认为同学甲的装置连接中不足以说明装置III中的现象是二氧化碳所为,请说出理由 ,在不增加其他装置和试剂,装置I、Ⅱ、Ⅲ可以重复使用的前提下,请提出修改方案,在修改方案中,装置I、Ⅱ、III的连接顺序为 (用“Ⅰ→Ⅱ→Ⅲ”的形式表示)。
查看答案和解析>>
科目: 来源: 题型:
聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·XH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:

(1) 反应中副产品a是 。
(2) 生产过程中操作A和操作B (填“是”或“否”)相同,有人建议在用清水清洗后也应该进行操作A,你认为他的建议 (填“是”或“否”)合理,理由是 ,操作A过程中使用到的主要玻璃仪器有 。
(3) 调节pH至4.0~4.5的目的是 。
(4) 实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到纯净的晶体。
生产过程C中可选用的物质为 (填字母代号) 。
A.NaOH B.Al C.氨水 D.Al2O3
查看答案和解析>>
科目: 来源: 题型:
下表为元素周期表的一部分,请回答有关问题:
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(1) ⑤和⑧两种元素名称分别是 和 ;
(2) 表中⑥的单核带两个负电荷离子的结构示意图为 ,该离子的半径 (填“大于”或“小于”)⑨的单核带一个正电荷离子的半径。
(3) 表中能形成两性氢氧化物的元素是 (填代号),分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应的水化物反应的化学方程式:
, ;
(4) 请设计一个实验方案,比较⑦、⑩两元素原子得电子能力的大小:
。
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分,有关说法正确的是

A.e的氢化物比d的氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.六种元素中,c元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z是短周期元素,但互不在同一个周期,且原子序数依次递增,X、Z同属于一个主族,三种元素可以形成原子个数比1:1:1的化合物。下列推测正确的是
A.三种元素中,Y的金属性最强
B.原子半径关系是:X<Y<Z
C.Y、Z都能形成含氧酸,且前者的酸性比后者酸性强
D.X、Y、Z形成的原子个数比1:1:1的化合物是共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com