
科目: 来源: 题型:
下列离子能在溶液中大量共存的是
A.Na+、NH4+、CO32-、Br- B.Fe2+、H+、ClO-、Cl-
C.Al3+、Ca2+、HCO3-、SO42- D.Fe3+、Cu2+、NO3-、OH-
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.水晶、玻璃、水泥都属于硅酸盐
B.乙烯、苯、甲苯都能使高锰酸钾溶液褪色
C.铝盐、活性碳、铁盐都常用作净水剂
D.SO2、H2O2、O3都可用作食品的漂白剂
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.![]() 的名称为2,2,4-三甲基-4-戊烯
的名称为2,2,4-三甲基-4-戊烯
B.化合物![]() 不是苯的同系物
不是苯的同系物
C.![]() 分子中所有碳原子一定共平面
分子中所有碳原子一定共平面
D.除甲酸外的羧酸均不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.C2H2的电子式为H:C:::C:H
B.酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
C.鸡蛋白溶液中滴加饱和硫酸铵溶液,出现沉淀,该过程属于蛋白质的盐析
D.6个碳原子形成的烃分子中,最多有5个碳碳单键
查看答案和解析>>
科目: 来源: 题型:
常温下0.1mol·L-1醋酸溶液的pH=a,下列能使溶液pH变为(a+1)的措施是
A.将溶液稀释到原体积的10倍 B.加入适量的醋酸钠固体
C.加入等体积0.2 mol·L-1盐酸 D.提高溶液的温度
查看答案和解析>>
科目: 来源: 题型:
下列有关物质的性质和该性质的应用均正确的是
A.常温下浓硫酸能使铝发生钝化,可在常温下用铝槽车贮运浓硫酸
B.二氧化硅不与任何酸反应,可用石英制造耐酸容器
C.二氧化氯具有还原性,可用于自来水的杀菌消毒
D.铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀
查看答案和解析>>
科目: 来源: 题型:
下列过程或事实不涉及氧化还原反应的是
①蔗糖炭化 ②用氢氟酸雕刻玻璃 ③铁遇冷的浓硫酸钝化
④装碱液的试剂瓶不用玻璃塞 ⑤雷雨发庄稼 ⑥浓硝酸常显黄色
A.①③⑤⑥ B.②④ C.②④⑥ D.①②③④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
下列有关生活中的化学的叙述中错误的是
①向燃料煤中加入生石灰,可以减少对大气的污染 [ :
②用双氧水清洗伤口,可以杀菌消毒
③只用淀粉溶液就能检验出食盐中是否加碘
④使用明矾可以对饮用水进行消毒、杀菌
⑤硫酸钡是一种难溶于水、难溶于酸的盐,可用作X光透视肠胃的内服药剂
A.①③④ B.①②⑤ C.③④ D.③④⑤
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.某温度( t℃)时水的离子积为1×10-13,若将此温度下pH=11的氢氧化钠溶液aL与pH=1的稀硫酸bL混合(混合后溶液总体积的变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比:
(1)若所得混合液为中性,则a:b= ;
(2)若所得混合液的pH=2,则a:b= 。
Ⅱ.在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH ![]()
![]() CH3CH3COO-+H+ △H>0,25℃时,该电离平衡的平衡常数为1.75×10-5。
CH3CH3COO-+H+ △H>0,25℃时,该电离平衡的平衡常数为1.75×10-5。
(1)25℃时,现有:①0.100mol·L-1 CH3COOH溶液②0.00100mol·L-1 CH3COOH溶液
其c(H+)之比为①:②= 。(提示:进行简化计算,平衡时的
c(CH3COOH)可用起始浓度代替,水电离出的c(H+)、c(OH-)忽略不计,下同)
(2)25℃时,向0.10mol·L-1 CH3COOH溶液中加入一定量固体CH3COONa(假设溶液体积不变),若溶液中c(CH3COO-)为1.0mol·L-1,则溶液中c(H+)= mol·L-1
(计算结果保留小数点后两位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。某化学兴趣小组在实验室条件下用硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。
步骤一:电解精制:
请回答以下问题:
电解时,粗铜应与电源的 极相连。阴极上的电极反应式为 。
电解过程中,硫酸铜的浓度会 (选填:变大、不变、变小)。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:
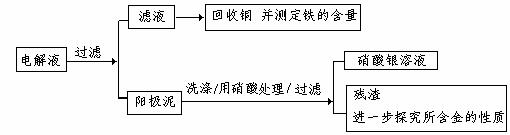
(1)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl— = AuCl4— | >>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸按体积比1∶3的混合物),请你简要解释金能够溶于王水的原因: 。
(2)滤液含量的测定:
以下是该小组探究滤液的一个实验流程:(已知氢氧化锌能溶于氢氧化钠溶液中)
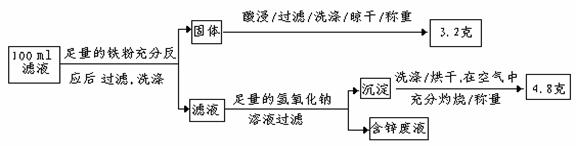
则100mL滤液中Cu2+ 的物质的量浓度为 ,Fe2+的物质的量浓度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com