
科目: 来源: 题型:
水溶液X中只可能溶有K+、Mg2+、Al3+、[Al(OH)4]-、SiO32-、SO32-、CO32-、
SO42-中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A.气体甲一定是纯净物
B.沉淀甲是硅酸和硅酸镁的混合物
C.K+、[Al(OH)4]-和SiO32-一定存在于溶液X中
D.CO32-和SO42-一定不存在于溶液X中
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.将Cl2通人FeBr2溶液中,溶液颜色变黄,则Fe2+被氧化,Br-不一定参加了反应
B.CO2、SO3、NO2和水反应均能生成相应的酸,都属于酸性氧化物
C.0.5 mol CH4完全燃烧生成CO2和液态水时,放出445kJ热量。其热化学方程式为
CH4 (g) +2O2(g)=CO2(g)+2H2O(g) △H=-890kJ/mol
D.分别由于![]() 和
和![]() 组成的金属钛单质互称为同分异构体,它们都有“生物金属”之称
组成的金属钛单质互称为同分异构体,它们都有“生物金属”之称
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z和W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在元素周期表中,Z与Y、W均相邻;Y、Z和W三种元素的原子最外层电子数之和为17。则下列有关叙述正确的是
A.Y、Z和W三种元素可能位于同一周期
B.上述元素形成的氢化物中, W的氢化物相对分子质量最大,熔、沸点最高
C.Y和W所形成的含氧酸均为强酸
D.X、Y、Z和W可以组成原子的物质的量之比为5∶1∶4∶1的离子化合物
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式正确的是
A.Fe(NO3)3溶液中加入过量的HI(强酸)溶液:2Fe3++2I-=2Fe2++I2
B.用惰性电极电解硫酸铜溶液:2Cu2++2H2O![]() 2H2↑+2Cu+O2↑
2H2↑+2Cu+O2↑
C.碳酸钡与稀硫酸反应:BaCO3+H2SO4 BaSO4+H2O+CO2↑
D.用小苏打治疗胃酸(盐酸)过多:HCO3- +H+ CO2↑+H2O
查看答案和解析>>
科目: 来源: 题型:
设NA表示阿伏加德罗常数的数值,下列说法正确的是
A.用石墨电极电解Ca(NO3)2溶液,当转移电子数为0.2 NA时,阴极析出4 g金属
B.0.1 mol24Mg32S晶体中所含中子总数为2.8 NA
C.常温下含有NA个NO2、N2O4分子的混合气体,温度降至标准状况,其体积约为22.4 L
D.在熔融状态下,1 mol NaHSO4完全电离出的阳离子数目为2NA
查看答案和解析>>
科目: 来源: 题型:
以下说法正确的是
A.共价化合物内部可能有极性键和非极性键 B.原子或离子间相互的吸引力叫化学键
C.非金属元素的原子间只能形成共价键 D.金属元素与非金属元素的原子间只形成离子键
查看答案和解析>>
科目: 来源: 题型:
化学与生产、生活、社会密切相关。下列有关说法中,错误的是
A.今夏,很多地区出现了严重的旱情,缓解旱情的措施之一是用碘化银进行人工增雨
B.新能源汽车的推广与使用有助于减少光化学烟雾的产生
C.利用太阳能、风能和氢能等能源替代化石能源有利于实现“低碳经济”
D.华商科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的单质硅
查看答案和解析>>
科目: 来源: 题型:
25℃时,0.1 mol·L-1的某酸HA溶液中![]() =1010,请回答下列问题:
=1010,请回答下列问题:
(1)HA是 酸(填“强”或“弱”),写出其电离方程式 。
(2)在加水稀释HA的过程中,随着水量的增加而减小的是________(填字母)。
A. ![]() B.
B.![]() C.c(H+)·c(OH-) D.c(OH-)
C.c(H+)·c(OH-) D.c(OH-)
(3)已知100℃时水的离子积是1.0×10—12,在此温度下,有pH=3的盐酸和pH=3的HA的两种溶液
①取等体积两溶液,分别稀释到pH=4时,两者加水量的关系是:前者________后者(填>、<或=,下同);
②取等体积的两溶液,分别加入等物质的量的相应钠盐固体少量,两溶液的pH大小关系是:前者________后者;
③50mL pH=3的盐酸溶液和50mL 0.003mol/LNaOH溶液混合后溶液的pH=_____________.
④pH=3的HA溶液中由水电离出的c(H+)= mol/L
(4)如何通过化学实验来证明HA是弱酸还是强酸,请写出其中的一种化学实验方法:
。
查看答案和解析>>
科目: 来源: 题型:
在某一容积为5 L的密闭容器内,加入
 0.3 mol的CO和0.3 mol的H2O,在催化剂存
0.3 mol的CO和0.3 mol的H2O,在催化剂存
在和800℃的条件下加热,发生如下反应:
CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH>0,反
CO2(g)+H2(g) ΔH>0,反
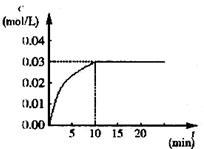
应中CO2的浓度随时间变化情况如右图:
(1)根据图上数据,反应开始至达到平衡时,
CO的化学反应速率为v(CO)= mol/(L·min)-1,
该温度下的平衡常数K= 。
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有
(填字母)
A.升高温度 B.降低温度 C.增大压强
D.减小压强 E.加入催化剂 G.移出一氧化碳气体
(3)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.2 mol的CO2和0.2 mol的H2,在相同的条件下,反应达平衡时,c(CO)=________________mol/L.
(4)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol 的水蒸气,重新达到平衡后,CO的转化率_______(填“升高”、“降低”还是“不变”),CO2的质量分数________(填“升高”、“降低”还是“不变”).
(5)在催化剂存在和800℃的条件下,在某一时刻测得C(CO)=C(H2O)= 0.09mol/L,
C(CO2 )=C(H2)=0.13mol/L ,则此反应是否处于平衡状态: (填“是”或“否”),若没有处于平衡状态则该反应向 移动。(填“正方向”或“逆方向”)
查看答案和解析>>
科目: 来源: 题型:
现有以下物质:①NaCl晶体, ②SO3, ③冰醋酸, ④铁丝,⑤BaSO4晶体,
⑥蔗糖,⑦乙醇,⑧熔融KNO3,请回答下列问题(填序号):
(1)以上物质中能导电的是 ;
(2)以上物质中属于非电解质,但其水溶液可以导电的是 ;
(3)以上物质中属于弱电解质的是 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com