
科目: 来源: 题型:
根据下列化合物:①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O,回答下列问题。
(1)NH4Cl溶液显________性,用离子方程式表示原因________,其溶液中离子浓度大小顺序为___________________。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=________,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=________。
(3)已知纯水中存在如下平衡:H2O+H2O ![]() H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是________(填字母序号)。
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是________(填字母序号)。
A.向水中加入NaHSO4固体 B.向水中加Na2CO3固体
C.加热至100℃[其中c(H+)=1×10-6mol·L-1] D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m________(填“<”、“>”或“=”)n。
(5)除⑧H2O外,若其余7种溶液的物质的量浓度相同,则这7种溶液按pH由大到小的顺序为:____________________(填序号)。
查看答案和解析>>
科目: 来源: 题型:
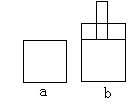
如图所示两个极易导热的密闭容器a和b,容器a体积恒定,容器b体积可变,在起始温度、体积相等的条件下,按下列两种情况投料。
Ⅰ、向a和b中充入等物质的量的NO2,发生反应:2NO2![]() N2O4;ΔH <0;
N2O4;ΔH <0;
Ⅱ、向a和b中充入等物质的量的N2O4,发生反应:N2O4![]() 2NO2;ΔH >0。
2NO2;ΔH >0。
以下判断对Ⅰ、Ⅱ两种情况均正确的是
A.反应起始时,两容器内反应速率va和vb的关系为:va = vb
B.反应过程中,两容器内反应速率va和vb的关系为:va<vb
C.反应达平衡时,两容器内反应物的转化率αa和αb的关系为:αa <αb
D.反应达平衡时,两容器内压强Pa和Pb的关系为:Pa>Pb
查看答案和解析>>
科目: 来源: 题型:
下列各项中的两个量,其比值一定为2∶1的是
A.液面在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛液体的体积
B.相同温度下,0.2 mol·L-1醋酸溶液和0.1 mol·L-1醋酸溶液中的c(H+)
C.在0.1 mol·L-1NaHSO4溶液中,阳离子数与阴离子数
D.在FeCl2溶液中,c(Cl—)与c(Fe2+)
查看答案和解析>>
科目: 来源: 题型:
常温下,将pH=1的H2SO4溶液平均分成两等份,一份加入适量水,另一份加入与该H2SO4溶液物质的量浓度相同的NaOH溶液,两者pH都升高了1,则加入的水和NaOH溶液的体积比为(假设混合前后溶液体积不变)
A.5:1 B.6:1 C.10:1 D.11:1
查看答案和解析>>
科目: 来源: 题型:
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的
A.溶液中导电粒子的数目减少
B.溶液中![]() 不变
不变
C.醋酸的电离程度增大,n(H+)亦增大
D.再加入10mlpH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目: 来源: 题型:
常温下有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的HCl溶液;③pH=11的氨水;④pH=11的NaOH溶液。下列说法正确的是
A.①与②中c(H+)相同
B.①与④混合,溶液中c(CH3COO-)=c(Na+) ks5u
C.②和③混合,所得混合溶液的pH大于7
D.③与④分别用等浓度的盐酸中和,消耗盐酸的体积相等
查看答案和解析>>
科目: 来源: 题型:
下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol·L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.1 L 0.1 mol·L-1 CuSO4·(NH4)2SO4的溶液中:c(SO![]() )>c(NH
)>c(NH![]() )>c(Cu2+)>c(H+)>c(OH-)
)>c(Cu2+)>c(H+)>c(OH-)
C.0.1 mol·L-1 NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO![]() )+c(OH-)
)+c(OH-)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
向CH3COONa稀溶液中加入(或通入)少许X物质,其溶液中部分微粒浓度变化如下表所示(溶液温度不变),则X物质可能是
| 微粒 | H+ | OH- | CH3COO- | CH3COOH |
| 物质的量浓度 | 增大 | 减小 | 减小 | 增大 |
A.氯化氢 B.氢氧化钠 C.蒸馏水 D.醋酸
查看答案和解析>>
科目: 来源: 题型:
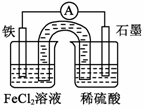
某原电池装置如右图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂。下列叙述正确的是
A.原电池工作一段时间后,FeCl2溶液中c(Cl-)会增大
B.Fe为负极,发生的反应为:Fe — 3e- = Fe3+
C.Fe为正极,石墨上发生的反应为:2H++2e-===H2↑
D.原电池装置中的盐桥完全可用金属导线代替
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com