
科目: 来源: 题型:
下列说法正确的是
A.酸性氧化物一定不能和酸反应
B.化学反应一定伴随着能量的变化
C.由同种元素组成的物质一定是纯净物
D.pH相同的两种酸溶液,水的离子积常数一定相等
查看答案和解析>>
科目: 来源: 题型:
生产、生活离不开各种化学物质,下列说法错误的是
A.不锈钢有较强的抗腐蚀能力是因为在钢铁表面镀上了铬
B.潜水艇在紧急情况下可用过氧化钠供氧
C.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
D.铝粉和氧化铁发生铝热反应可焊接钢轨
查看答案和解析>>
科目: 来源: 题型:
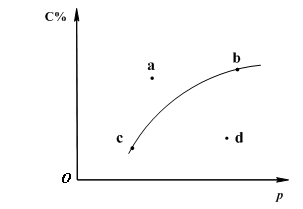
对于可逆反应2A(?)+B(g)![]() 2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
(1)物质A的状态是 (填“气体”、“液体”或“固体”);
(2)图-1中a、b、c、d四点中表示未达到平衡状态且v正<v逆 的点是 ;
(3)在a、b、c三种条件下达平衡时,v(a)、v(b)、v(c)按由大到小排序___________;
 |
|
(4)对于2SO2(g)+O2(g)![]() 2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
请问原料气中SO2与O2的体积比不是2∶1,而要7∶11(大约2∶3)的原因是
;如果在恒容容器中,仅把另外82%的其他气体“抽出来”,是否会减小SO2的转化率 (填“会”或“不会”)。
查看答案和解析>>
科目: 来源: 题型:
25℃,浓度都是1mol/L的四种正盐溶液,其pH情况如下:
| AX | BX | AY | BY |
| pH=7,c(X—)=1mol/L | pH=4 | pH=6 |
(1)AY溶液pH______7 (填“>”、“<”或“=”);
(2)将等浓度的HX、HY稀释相同的倍数,溶液的pH变化幅度:HX HY;若将等体积、等pH的AOH、BOH溶液在稀释时pH均下降2,则加水量:AOH BOH(均填“>”、“<”或“=”);
(3)在BX溶液中:c(B+)+c(H+)-c(OH-)=________mol/L;
在AY溶液中:c(A+)-c(Y-)=________(用一项表示)=___________(用两项表示);
(4)A2Z的水解方程式是_____________________________________________;__________________________________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
(1)硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因_______________________________________,如何才能用热水配制出澄清的较浓的CuSO4溶液____________________________;
(2)稀Na2S溶液有一种腐卵气味,加入AlCl3溶液后,腐卵气味加剧,用离子方程式表示气味加剧过程所发生的化学反应________________________________________。
(3) 下列物质水溶液经加热浓缩、蒸干灼烧后能得到原溶质物质的是____________
①NH4HCO3;②CaCl2;③AlCl3;④Cu(NO3)2;⑤FeCl2;⑥K2SO3;⑦KMnO4;⑧KAl(SO4)2
Ⅱ.(6分)依据氧化还原反应:MnO4-+5Fe2++8H+ = Mn2++5Fe3++4H2O,欲采用滴定的方法测定FeSO4的质量分数,实验步骤如下:
①称量绿矾样品,配成100 mL待测溶液,②取一定体积待测液置于锥形瓶中,并加入一定量的硫酸,③将标准浓度的KMnO4溶液装入滴定管中,调节液面至a mL处,④滴定待测液至滴定终点时,滴定管的液面读数b mL,⑤重复滴定2~3次。
(1)如何知道滴定到达终点? _ 。
下列操作会导致测定结果偏低的是 。
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(2)下列每种量器的数量不限,在上述实验中,必须使用的有 ;
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管
查看答案和解析>>
科目: 来源: 题型:
在25℃时,恒容密闭容器中X、Y、Z三种气体的初始物质的量和平衡物质的量如下:
| 物质 | X | Y | Z |
| 初始物质的量/mol | 0.1 | 0.3 | 0 |
| 平衡物质的量/mol | 0.05 | 0.2 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+2Y![]() 2Z
2Z
C.若起始时X、Y、Z的物质的量分别为0.1 mol、0.4mol、0.2 mol,达平衡时,Z的体积分数一定增大
D.若起始时X、Y、Z的物质的量分别为0.05 mol、0.15mol、0.1mol,达平衡时,X的转化率一定与原投料相等。
查看答案和解析>>
科目: 来源: 题型:
下图是可逆反应A+2B![]() 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
A.若A、B是气体,则D是液体或固体
B.A、B、C、D均为气体
C.逆反应是放热反应
D.达平衡后,v(A)正 =2 v(C)逆

查看答案和解析>>
科目: 来源: 题型:
关于下列室温下的溶液的一些说法中,完全正确的是
①pH=4 FeCl3溶液;②pH=10 Na2CO3溶液;③pH=2 HCl溶液;④pH=3 CH3COOH溶液;⑤pH=11 NaOH溶液;⑥pH=3 NH4Cl溶液
A.水的电离程度:①=②、③<④、⑤=⑥
B.④、⑤溶液等体积混合后所得溶液中水的电离程度大于纯水的电离程度
C.⑤、⑥溶液等体积混合后所得溶液中离子浓度顺序是c(Cl—)>c(NH4+)>c(OH—)>c(H+)
D.②溶液中:c(H+)+c(H2CO3)+c(HCO3—)=c(OH—)
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.已知30℃时Kw=3.80×10-14,则30℃时c(H+)=1.00×10-7mol/L的溶液是酸性的
B.正常成人胃液的pH=1.4,婴儿(体温与成人相同)胃液的pH=5.0,鉴于人的正常体温不是25℃,故两种胃液的c(OH—)不可能相差103.6倍
C.新制氯水中加入少量的NaHSO3晶体不会使c(HClO)增大
D.在熔融状态下,1molKHSO4完全电离出的阳离子数目为2NA
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是
A.等体积等浓度的Na2S溶液和Na2SO3溶液中,离子数目以前者为多
B.已知室温时0.10mol/L NH4Cl溶液中c(H+) =7.5×10-6mol/L,室温时0.10mol/L KCN溶液中c (OH—) =1.3×10-3mol/L。那么此时0.10mol/L NH4CN溶液中pH>7
C.等pH、等体积的醋酸和硫酸,分别与足量的碳酸氢钠反应,在相同条件下,硫酸放出气体更多
D.醋酸加到氢氧化钠溶液中,若要使所得溶液呈中性,醋酸应稍过量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com