
科目: 来源: 题型:
下列叙述正确的是( )
A.过量的Fe粉与氯气和氯水反应所得氯化物相同
B.Na、Mg、Al分别与不足量的稀硫酸反应所得溶液均呈中性
C. 铁粉中混有铝粉既可用过量的NaOH溶液,也可以用过量FeCl3充分反应过滤除去
D.常温下,铝制品用浓硫酸或浓硝酸处理过,可耐腐蚀
查看答案和解析>>
科目: 来源: 题型:
某学生用NaHCO3和KHCO3组成的某化合物进行试验,测得如下数据(盐酸的物质的量浓度相等):
| 实验编号 | ① | ② | ③ |
| 盐酸体积 | 50mL盐酸 | 50mL盐酸 | 50mL盐酸 |
| m(混合物) | 9.2g | 16.56 g | 27.6 g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
根据表中数据试计算:
(1)盐酸的物质的量浓度。
(2)混合物中NaHCO3的质量分数。
查看答案和解析>>
科目: 来源: 题型:
维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量![]() 可通过在其弱酸性溶液中用I2溶液进行滴定。
可通过在其弱酸性溶液中用I2溶液进行滴定。
该反应的化学方程式为:C6H8O6+I2=C6H6O6+2HI
现欲![]() 测定某样品中维生素C的含量,具体的步骤及测得的数据如下:
测定某样品中维生素C的含量,具体的步骤及测得的数据如下:
①取10mL6mol·L-1CH3COOH,加入100mL蒸馏水,将溶液加热煮沸后放置冷却。
②准确称取0.2000g样品,溶解于上述冷却的溶液中,并加入1mL淀![]() 粉指示剂。
粉指示剂。
③随后,立即用浓度为0.0500 mol·L-1的I2溶液进行滴定,直至溶液中的蓝色持续不褪为止,共消耗21.00mLI2溶液。
(1)为何加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用?
①煮沸的原因
②冷却后才能使用的原因
(2)经过计算,样品中维生素C的百分含量为
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2 mL乙醇的试管里,反复操作几次。
请你评价若用上述方法制取乙醛存在哪些不足(写出两点)。
。
Ⅱ.某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白:
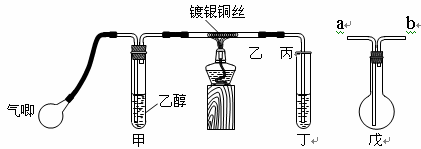
(1) 甲装置常常浸在70~80℃的水浴中,目的是
。
(2)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。
①乙醇的催化氧化反应是________反应(填“放热”或“吸热”),该反应的化学方程式为 。
②控制鼓气速度的方法是 ,若鼓气速度过快则会 ,若鼓气速度过慢则会 。
(3)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接 、_______接丙;若产物不用水吸收而是直接冷却,应将试管丁浸在 _____ 中。
查看答案和解析>>
科目: 来源: 题型:
化合物A、B、C都只含有两种元素,且A、B均含X元素。已知一定条件下可发生反应:A+B——X+C,X是一种单质,由![]() 此可知X元素 ( )
此可知X元素 ( )
A.一定是金属元素 B.一定是非金属元素
C.可能是金属元素,也可能是非金属元素 D.无法确定
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式正确的是( )
A.少量的钠跟足量盐酸反应:2Na+2H2O=2Na++2OH-+H2↑
B.过量Cl2通向湿润的淀粉KI试纸,先变蓝后褪去:Cl2+2I-=2Cl-+I2
C.Ba(HCO3)2溶液与Ba(OH)2溶液任意比混合:Ba2++HCO3-+OH-=BaCO3↓+H2O
D.向浓HNO3溶液中加入足量的铁粉:Fe+2NO3-+4H+=Fe2++2NO2↑+2H2O
查看答案和解析>>
科目: 来源: 题型:
如图的分子酷似企鹅,化学家 Chris Scotton将该分子以企鹅来取名为Penguinone。下列有关Penguinone的说法不正确的是 ( )
A. Penguinone分子中有碳原子不可能都在同一个平面上
B. Penguinone的分子式为C10H14O,且能使溴水褪色
C. 1 mol Penguinone完全燃烧消耗13 mol O2
D. Penguinone的同分异构体中属于酚类只含有一个烃基侧链的物质共有4种

查看答案和解析>>
科目: 来源: 题型:
下列有关判断正确的是( )
A.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+3OH-=Al(OH)3
C.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+
D.用原电池和电解池装置都能实现2HCl + Cu=CuCl2 + H2↑ 反应
查看答案和解析>>
科目: 来源: 题型:
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发![]() 生如下两个反应:
生如下两个反应:
2Fe![]() H2O2
H2O2![]() 2H
2H![]() → 2Fe
→ 2Fe![]() 2H2O 2Fe
2H2O 2Fe![]() H2O2 → 2Fe
H2O2 → 2Fe![]() O2↑
O2↑![]() 2H
2H![]()
下列说法正确的是( )
A.H2O2的氧化性比Fe![]() 强,其还原性比Fe
强,其还原性比Fe![]() 弱
弱
![]() B.在H2O2分解过程中,溶液的pH逐渐下降
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中,Fe![]() 和Fe
和Fe![]() 的总量保持不变
的总量保持不变
D.H2O2生产过程要严格避免混入Fe![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com