
科目: 来源: 题型:
下列说法中,正确的是( )
A.强电解质溶液一定比弱电解质溶液导电能力强
B.不溶性盐是弱电解质
C.强电解质的水溶液中不存在溶质分子
D.因为醋酸是弱电解质,盐酸是强电解质,因此中和等体积等物质的量浓度的醋酸和盐酸时,中和盐酸消耗的氢氧化钠比中和醋酸多
查看答案和解析>>
科目: 来源: 题型:
下列有关防护金属腐蚀的说法中,不正确的是( )
A.青铜(锡铜合金)中的锡可对铜起保护作用
B.在海轮外壳上焊接上锌块,可减缓船体的腐蚀速率
C.海水中钢闸门与电源的正极相连,可以防止闸门的腐蚀
D.钢铁表面烤蓝生成一层致密的Fe3O4,能起到防腐蚀的作用
查看答案和解析>>
科目: 来源: 题型:
将25.6g的铜投入200mL物质的浓度为3 mol·L-1稀硝酸中
(1)该反应的离子方程式 (2)生成气体在标况下的体积为
(3)往反应后的溶液中加入足量的稀硫酸,充分反应后,溶液中的铜离子的物质的量浓
度为 (假设反应前后溶液体积不变)(注:2、3步骤写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
(1)将样品研细的目的是:
(2)步骤②加入过量H2O2的目的是:
能证明该反应已进行完全的试剂是 K^S*5U.C#O%
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性![]() 溶液
溶液
(3)步骤③中若X为氨水,则反应的离子方程式为:
(4)步骤④中一系列处理的操作步骤:过滤、 、灼烧、冷却、称量。
(5)若实验无损耗,则该样品中含铁元素的质量 g(用含a的代数式表示,不用化简)。
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定,反应原理如下:
□Fe2+ + □MnO4— + □ →□Fe3+ +□Mn2+ +□H2O
试完成并配平上述离子方程式
查看答案和解析>>
科目: 来源: 题型:
工业上常用铝质容器盛装冷浓酸。为研究铝质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)将铝片放入氢氧化钠溶液中以除去表面氧化膜,反应的离子方程式为
(2)将已去除表面氧化物的铝片放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铝片表面无明显变化,其原因是 。
(3)另称取铝片6.0g放入15.0mL浓硫酸中,加热,充分应后收集到气体X 。甲同学取448ml(标准状况)气体X通入足量过氧化氢溶液中,然后再加入足量![]() 溶液,经适当操作后得干燥固体2.33g ,由于此推知气体X中
溶液,经适当操作后得干燥固体2.33g ,由于此推知气体X中![]() 的体积分数为 。
的体积分数为 。
[探究二]
分析上述实验中![]() 体积分数的结果,丙同学认为气体X中还可能含量有
体积分数的结果,丙同学认为气体X中还可能含量有![]() 。为此设计了下列探究实验装置(图中夹持仪器省略)。
。为此设计了下列探究实验装置(图中夹持仪器省略)。
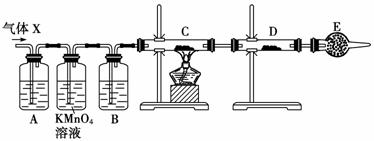
(1)丙同学认为还可能产生氢气的理由是_________________________________ _ 。
(2)A中试剂可选用( )
a.高锰酸钾溶液 b.品红溶液 c.氢氧化钠溶液 d.溴水
(3)B中加入的试剂可能是 ,E的作用是___________________ ;
(4)可以证明气体X中含有氢气的实验现象是:
________________________________________ _。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
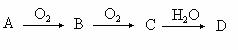
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途
(2)若A为淡黄色固体单质,写出B→C转化的化学方程式
(3)若A为单质,D为弱酸,则A在工业生产中可用于制备另一种非金属单质,该反应的化学方程式为
(4)若C是红棕色气体,则A的化学式可能为 。C转化为D的过程中,氧化剂与还原剂的质量比为
查看答案和解析>>
科目: 来源: 题型:
把a g铁铝合金粉末溶于足量的盐酸中,加入过量氢氧化钠溶液,过滤出沉淀,经洗涤、干燥、灼烧,得到红色粉末的质量仍为a g,则原合金中铝的质量分数为( )
A. 70% B. 52.4% C. 47.6% D. 30%
查看答案和解析>>
科目: 来源: 题型:
一定质量的铜分别与足量的浓HNO3和稀HNO3完全反应,在相同条件下用排水法收集反应产生的气体,下列叙述正确的是
A.浓度越大,消耗的硝酸越少
B.硝酸浓度不同,生成的Cu(NO3)2的物质的量不同
C.硝酸浓度越大,产生的气体越少
D.两者用排水法收集的气体体积相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com