
科目: 来源: 题型:
美国《科学》杂志评出2001年十大科技成就,名列榜首的是纳米电子学,其中美国一家公司制造的第一批纳米碳管晶体管,发明了种用电子的波性来仁慈信息的“导线”已知纳米材料是指微粒直径在1-100nm的材料。下列叙述正确的是( )。
A.纳米碳管是一种新型的高分子化合物 B.纳米碳管的化学性质稳定
C.纳米碳管的结构和性质与金刚石相同 D.纳米碳管导电属于化学变化
查看答案和解析>>
科目: 来源: 题型:
下列关于工业生产说法正确的是( )
A.在侯氏制碱工业中,向饱和氯化钠溶液中先通氨气,后通二氧化碳]
B.在硫酸工业、合成氨工业、硝酸工业中,均必须对尾气进行吸收处理
C.工业上用电解熔融氧化物的方法制金属镁和铝
D.氯碱工业中的阳离子交换膜阻止阳离子通过
查看答案和解析>>
科目: 来源: 题型:
食品香精菠萝酯的生产路线(反应条件略去)如下,下列叙述错误的是( )

A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B.反应(1)和(2)均为取代反应
C.苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应,均有酸性。
D.与苯氧乙酸互为同分异构体,能使FeCl3溶液显紫色,并能发生水解反应但不发生银镜反应的芬香族化合物共有6种
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是( )
A.汽油、柴油和植物油都是碳氢化合物
B.利用核磁共振氢谱图可鉴别1-溴丙烷和2-溴丙烷
C.甲烷、乙烯和苯在工业上都可通过石油分馏得到
D.含5个碳原子的有机物,每个分子中最多可形成4个C-C单键
查看答案和解析>>
科目: 来源: 题型:
硅橡胶是一种新型橡胶,它是由二甲基二氯硅烷经过两种类型的反应而形成的高分子化合物。则这两种反应为( )
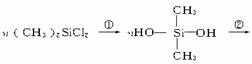
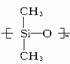
A.消去,加聚 B.氧化,聚合 C.水解,加聚 D.水解,缩聚
查看答案和解析>>
科目: 来源: 题型:
有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸。某研究性学习小组的同学们利用一小块样品,进行了以下实验。
(1)检验矿物样品中是否有Fe3+
实验用品:锤子、研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
实验步骤:①取样:将样品用锤子敲碎,再在研钵中研细备用。
②溶解:将样品粉末倒入烧杯,加入 ,用玻璃棒充分搅拌。
③过滤。
④检验:取少许滤液于试管中,滴加 。实验现象: 。
实验结论:矿物样品中含有Fe3+。
(2)制备氢氧化亚铁
① 为了得到亚铁盐的溶液,同学们在剩余的溶液中加入过量的某种固体试剂,该试剂是(填化学式) ,反应的离子方程式是 。
② 同学们在新制得的亚铁盐溶液中加入不含O2的蒸溜水配制的NaOH溶液,制出的氢氧化亚铁。)其操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。要这样操作的理由是_____ 。
写出氢氧化亚铁和氧气反应的化学方程式: 。
查看答案和解析>>
科目: 来源: 题型:
铝土矿的主要成分是![]() ,含有杂质
,含有杂质![]() 、
、![]() 、
、![]() 。工业上从铝土矿中提取铝可采用如下工艺流程:
。工业上从铝土矿中提取铝可采用如下工艺流程:

请回答下列问题:(1)图中涉及分离溶液与沉淀的实验方法是_________(填操作名称)。
(2)沉淀B的成分是____________(填化学式,下同),沉淀C的成分是____________;溶液D中所含的酸根离子是 。
(3)沉淀F转化为物质M的化学方程式为________________________;
溶液D中通入过量![]() 生成沉淀F的离子方程式为_______________________。
生成沉淀F的离子方程式为_______________________。
(4)能否将向溶液D中通入过量![]() 换成加入过量盐酸? (填 能 或 不能)
换成加入过量盐酸? (填 能 或 不能)
其理由是 (2分)
查看答案和解析>>
科目: 来源: 题型:
氯化钠、氢氧化钠 、碳酸钠和碳酸氢钠是生活中常见的物质。
请回答下列问题。
(1)粗盐中含有可溶性CaCl2、MgCl2 Na2SO4杂质,除去这些杂质的试剂可选用
①Na2CO3、②NaOH、③BaCl2、④ HCl ,加入试剂的先后顺序可以是
(2)等质量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者 后者
(填 >、< 或 =)。
(3)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
。
(4) 除去NaHCO3溶液中的少量Na2CO3,方法是:
离子方程式: 。
(5)钠与氢气在加热条件下能发生反应,生成一种白色固体。其中氢元素的化合价为-1价,写出白色固体与水剧烈反应生成氢气的化学方程式为
查看答案和解析>>
科目: 来源: 题型:
请按要求回答下列问题:
(1).某合作学习小组讨论辨析以下说法,其中说法正确的是 _____________
A根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸等
B 将Na2O2投入FeCl2溶液中, 可观察到的现象是生成红褐色沉淀、有气泡产生
C 金属元素的原子只有还原性,离子只有氧化性
D不锈钢和目前流通的硬币都是合金;
E NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质
(2)将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为_____________
(3)在K2Cr2O7+14HCl==2KCl+2CrCl3+3Cl2↑+7H2O反应中,
氧化剂是_____ _(填化学式) 当有14.6gHCl被氧化时,电子转移为 mol。
(4)学校研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其他元素)中镁的质量分数,设计下列实验方案进行探究,填写下列空白:
实验方案:铝镁合金 ![]()
![]() 测定剩余固体质量。
测定剩余固体质量。
① 实验中发生反应的化学方程式是__________________。
② 实验步骤:称取5.4 g铝镁合金粉末样品,投入V mL 2.0 mol/L NaOH 溶液中充分反应。计算所用NaOH溶液的体积V≥______________。
过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将________( 填 不变 偏高 或 偏低 )。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com