
科目: 来源: 题型:
科学家最近制造出第112号新元素,其原子的质量数为277,关于该新元素的下列叙述正确的是
A. 其原子核内中子数和质子数都是112
B.其原子核内中子数为165,核外电子数为112
C.其原子质量是12C原子质量的277倍
D.该元素在周期表中位于七周期IVA族
查看答案和解析>>
科目: 来源: 题型:
避蚊酯(DMP)是一种塑化剂.相对分子质量为194,摄人后对人体有一定的危害,其结构可表示为![]() (其中R为烃基)实验室由以下方法可得到DMP:
(其中R为烃基)实验室由以下方法可得到DMP:
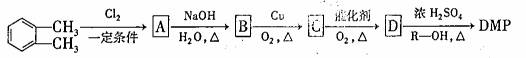
请回答:
(1)物质C中官能团的名称为 。
(2)下列有关DMP的说法可能正确的是 。(填字母标号)
A.DMP的分子式为C10H12O4
B.DMP可以发生取代、加成、氧化等反应
C.DMP在水中的溶解度不大
(3)B与乙二酸(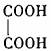 )在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分
)在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分
子化合物的结构简式为 。
(4)工业上以邻二甲苯(![]() )为原料先生产苯酐(
)为原料先生产苯酐(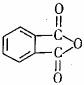 ),再使其与某醇在 一定条件下反应制取DMP。苯酐与该醇制取DMP的化学方程式为 。
),再使其与某醇在 一定条件下反应制取DMP。苯酐与该醇制取DMP的化学方程式为 。
(5)芳香化合物E与C互为同分异构体,若lmo E与足量银氨溶液反应取多2mol Ag,则E可能的结
构简式为 。B也存在多种同分异构体,符合下列条件的B的同分异构体有 种。
① lmol有机物可以与2mol NaOH反应②苯环上的一氯代物只有一种
查看答案和解析>>
科目: 来源: 题型:
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·xH2O)。

(1)实验室采用如图所示装置,可使粗铜与Cl2反应转化为固体1(部分加热仪器和夹持装置已略去)。该装置中仪器a的名称是 。装置b中发生反应的离子方程式是 。
该装置存在一定的安全隐患,消除该安全隐患的措施是 。

(2)操作Ⅱ中应控制的pH范围为 ,其目的是 。
已知:

(3)操作Ⅲ的程序依次为 、 、过滤、自然干燥.得到CuCl2·xH2O晶体。
(4)若制备的氯化铜晶体经检验含有FcCl2,其原因可能是 ,
试提出两种不同的改进方案:① ;
② 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:
![]() ,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响。)

 ①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是 。
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是 。
②实验过程中,需要通入氧气。试写出一个用右图所示装置制取氧气的化学方程式 。
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是 。
 ④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是 (用含字母的代数式表示,不用化简)。
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是 (用含字母的代数式表示,不用化简)。
(3)某学习小组设计用如右图装置验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是 (填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为 。
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)= (用含硫微粒浓度的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
化学反应原理在工业生产中具有十分重要的意义。
(1) 合成氨用的氢气有多种制取方法:请你写出用C制备水煤气的化学反应方程式
。
还可以由天然气或重油制取氢气:![]() ;比较以上两种方法转移6mol电子时,C和CH4的质量之比是 。
;比较以上两种方法转移6mol电子时,C和CH4的质量之比是 。
(2)工业生产可以用NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为 。
(3)已知反应![]() 。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
。测得在不同温度下,该反应的平衡常数K随温度的变化如下:

①该反应的化学平衡常数表达式K= ,a 0(填“>”、“<”或“:”)。在500℃2L密闭容器中进行反应,Fe和CO2的起始量均为4 mol,则5min后达到平衡时CO2的转化率为 ,
生成CO的平均速率v(CO)为 。
②700℃反应达到平衡后,要使该平衡向右移动,其他条件不变时,可以采取的措施有 (填字母)。
A.缩小反应器容积 B.增加Fe的物质的量
C.升高温度到900℃ D.使用合适的催化剂
查看答案和解析>>
科目: 来源: 题型:
用下列实验装置进行相应实验,能达到实验目的是

A.用图1所示装置除去HCI气体中的少量C12 B.用图2所示装置检验加热时产生的乙烯
C.用图3所示装置在铁制品表面镀铜 D.用图4所示装置分离溴的四氯化碳溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com