
科目: 来源: 题型:
已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平。
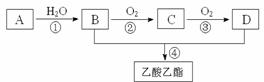 现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
(1)A在一定条件下可以聚合生成一种常见塑料,该塑料的结构简式为 ▲ 。
(2)反应④的化学方程式为 ▲ 。
(3)按要求回答:
①、④的反应类型为 ▲ 、 ▲ ,②的反应条件为 ▲ 。
(4)在实验室中获得的乙酸乙酯往往含有B、D,为提纯E,加入的试剂以及分离操作方法是▲、▲。
(5)假设①②③步转化率都是100%,第④步转化率是60%,则用标准状况下4.48×105 m3的A,经
过上述步骤理论上最多能生产出乙酸乙酯 ▲ 吨。
查看答案和解析>>
科目: 来源: 题型:阅读理解
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、
减少酸雨和光化学烟雾的有效途径。
⑴ 有效“减碳”的手段之一是节能。下列制氢方法最节能的是 ▲ 。(填字母序号)
A.电解水制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O![]() CO+3H2
CO+3H2
⑵ CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 molCO2和3 mol H2,一定
条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,测得CO2 和CH3OH(g)
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,测得CO2 和CH3OH(g)
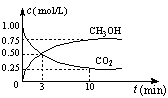
的浓度随时间变化如下图所示。
①从3 min到10 min,v(H2)= ▲ mol·L-1·min-1。(保留2位有效数字)
 ②能说明上述反应达到平衡状态的是 ▲ (选填编号)。
②能说明上述反应达到平衡状态的是 ▲ (选填编号)。
A.反应中CO2与CH3OH的物质的量浓度相等
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
⑶ 新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产
物反应。该技术的优点除了能回收利用SO2外,还能得到一种正盐作为复合肥料。该复合肥料的化
 学式为 ▲ 。
学式为 ▲ 。
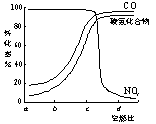
⑷ 在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、
NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。某研究性学习小组探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 ▲ 时,催化剂对汽车尾气的催化效果最好。(填a、b、c、d)
查看答案和解析>>
科目: 来源: 题型:
(1)某同学设计了如下实验流程:在一个小烧杯里,加入20g Ba(OH)2·8H2O晶体和10gNH4Cl晶体,
然后将小烧杯放在事先已滴有3滴~4滴水的玻璃片上,并立即用玻璃棒迅速搅拌。实验流程示意图
如下,回答下列问题:

①实验中玻璃棒的作用是 ▲ 。
②浸有稀硫酸的棉花的作用是 ▲ 。
③通过 ▲ 现象,说明该反应为 ▲ (填“吸热”或“放热”)反应,这是由于反应物的
总能量 ▲ (填“小于”、 “大于” 或“等于”)生成物的总能量。
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生
沼气,可用来点火做饭。在农村推广建造沼气池,不仅能有效地利用 ▲ 能,还能为农业生产提
供优良的肥料。已知: 标准状况下的112.0L CH4气体完全燃烧,生成CO2和液态水,放出4448kJ
的热量。
①写出CH4完全燃烧的热化学方程式为 ▲ 。
②如果上述反应生成的是水蒸气,则反应放出的热量 ▲ 4448kJ。(填“>”或“<”或“=”)
(3)钢铁在潮湿的空气中生锈主要是由电化学腐蚀造成的,发生腐蚀时铁和内部的杂质碳及钢铁表
面的电解质溶液形成原电池。钢铁发生电化学腐蚀时铁作为原电池的 ▲ 极,此电极反应式为
▲ 。
查看答案和解析>>
科目: 来源: 题型:
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,回答下列问题:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)③、④、⑧的原子半径由大到小的顺序为 ▲ (用元素符号回答)。
(2)⑤、⑥、⑦的最高价氧化物对应的水化物碱性由强到弱的顺序是 ▲ 。(用化学式回答)
(3)②、⑨两种元素形成的某化合物是一种常见的有机溶剂,写出该化合物的电子式 ▲ 。
(4)④和⑧形成的化合物属于 ▲ 晶体(填“离子”、“分子”、“原子”),该晶体中微粒间的作用力为 ▲ 。
(5)②形成的单质与③形成的最高价氧化物的水化物的浓溶液反应的化学方程式 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L—1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60 mL B.45 mL C.30 mL D.15 mL
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是
A.X的原子半径大于Y的原子半径B.W的最高价氧化物对应水化物的酸性比Z的强
C.Z的非金属性比Y的强
D.X与Y形成的化合物都易溶于水
![]()
查看答案和解析>>
科目: 来源: 题型:
关于下列各装置图的叙述中,正确的是
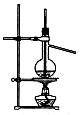
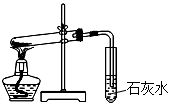
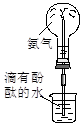
① ② ③ ④
A.实验室用装置①探究NH4Cl的热稳定性 B.装置②用于证明氨气极易溶于水
C.装置③用于石油的分馏 D.装置④用于乙酸乙酯的制备
查看答案和解析>>
科目: 来源: 题型:
巴豆酸是一种对胃肠道有强烈刺激性、对呼吸中枢和心脏有麻痹作用的有机酸,其结构简式为
CH3—CH=CH—COOH,现有①氯化氢 ②溴水 ③纯碱溶液 ④乙醇 ⑤酸性高锰酸钾溶液试根据其结构特点判断在一定条件下能与巴豆酸反应的物质是
A.只有②④⑤ B.只有①③④ C.只有①②③④ D.全部

查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1mol CH3+(碳正离子)中含有电子数为10NA
B.用石墨电极电解氯化铜溶液时,若阴极增重64 g,则电路中转移的电子数为2 NA
C.常温常压下,22.4 L乙烷中含有的共价键数为7 NA
D.在密闭容器中,1molN2与3molH2在一定条件下充分反应,生成氨气的分子数为2 NA
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式正确的是
A.向盐酸中加入适量氨水:H++OH-=H2O
B.铁与足量稀HNO3反应:3Fe+ 8H++2NO3-=3 Fe 2++2NO↑+4H2O
C.氢氧化铜溶于硝酸:2H++Cu(OH)2=Cu2+ +2H2O
D.铜与浓HNO3反应:Cu+4H++2NO3- = Cu2+ +2H2O+2NO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com