
科目: 来源: 题型:
在pH=1的无色溶液中,下列离子能大量共存的是 ( )
A.NH4+、Ba2+、NO3—、CO32— B.Fe2+、OH—、SO42—、MnO4—
C.K+、Mg2+、NO3-、SO42— D.Na+、Fe3+、Cl—、AlO2—
查看答案和解析>>
科目: 来源: 题型:
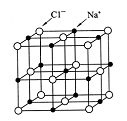
右图是氯化钠晶体的结构示意图,其中,与每个Na+距离最近且等距离的几个Cl-所围成的空间的构形为( )
A.正四面体形 B.正六面体形 C.正八面体形 D.三角锥形
查看答案和解析>>
科目: 来源: 题型:
常温常压下为无色液体,而且密度大于水的是( )
①一氯甲烷 ② 硝基苯 ③ 溴苯 ④ 四氯化碳 ⑤ 溴乙烷 ⑥ 乙酸乙酯
A. ①⑥ B. ②③④⑥ C. ②③④⑤ D. ①④⑤
查看答案和解析>>
科目: 来源: 题型:
下列说法中不正确的是 ( )
A. 维勒用无机物合成了尿素,突破了无机物与有机物的界限
B. 开发核能、太阳能等新能源,推广乙醇汽油,使用无磷洗涤剂都可直接降低碳排放量
C. 红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析
D. 尼龙、棉花、天然橡胶、ABS树脂都是由高分子化合物组成的物质
查看答案和解析>>
科目: 来源: 题型:
硝酸与金属反应时,浓度越稀还原产物价态越低。现用一定量的铝粉与镁粉组成的混合物与100ml硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,相反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与与产生的沉淀质量的关系如图所示。


回答下列问题:
(1)写出铝与混合溶液反应的离子方程式:
(2)参加反应硝酸根离子物质的量为 mol
(3)参加反应的铝与镁的质量比为
(4混合液中硫酸的物质的量的浓度为 mol/L
查看答案和解析>>
科目: 来源: 题型:
工业废水中常含有一定量的Cr2O![]() 和CrO
和CrO![]() ,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法。该法的工艺流程为CrO![]()
![]() Cr2O
Cr2O![]()
![]() Cr3+
Cr3+![]() Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO![]() (黄色)+2H+
(黄色)+2H+![]() Cr2O
Cr2O![]() (橙色)+H2O
(橙色)+H2O
(1)若平衡体系的pH=2,该溶液显________色。
(2)能说明第①步反应达平衡状态的是__________。
a.Cr2O![]() 和CrO
和CrO![]() 的浓度相同
的浓度相同
b.2v(Cr2O![]() )=v(CrO
)=v(CrO![]() )
)
c.溶液的颜色不变
(3)第②步中,还原1 mol Cr2O![]() 离子,需要________mol的FeSO4·7H2O。
离子,需要________mol的FeSO4·7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) ![]() Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至________。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至________。
方法2:电解法。
该法用Fe做电极电解含Cr2O![]() 的酸性废水,
的酸性废水,
随着电解进行,在阴极附近溶液pH升高,产
生Cr(OH)3沉淀。
(5)用Fe做电极的原因为__________________。
(6)在阴极附近溶液pH升高的原因是(用电极反
应解释)_________________________________。
溶液中同时生成的沉淀还有__________。
查看答案和解析>>
科目: 来源: 题型:
下图是工业生产硝酸铵的流程。
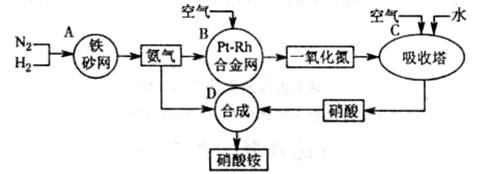
(1)吸收塔C中通入空气的目的是 。A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) +6H2O(g) △H =-1266.8kJ/mol
N2(g) + O2(g) = 2NO(g) △H = +180.5 kJ/mol
写出氨高温催化氧化的热化学方程式: 。
(3)已知:N2(g) +3H2(g) ![]() 2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有 (填字母)。
2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有 (填字母)。
A.升高温度 B.使用催化剂 C.增大压强 D.循环利用和不断补充氮气
(4)在一定温度和压强下,将H2和N2按3 : 1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,求此时H2的转化率?(要有完整的计算过程,结果保留三位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com