
科目: 来源: 题型:
下列表示对应化学反应的离子方程式正确的是( )
A.漂白粉露置在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
B.向滴有酚酞的硅酸钠溶液中边加边振荡地滴加盐酸至红色变浅并接近消失: 2H++SiO32-=H2SiO3(胶体)
C.向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO-+Fe(OH)3= FeO42-+3Cl-+H2O+4H+
查看答案和解析>>
科目: 来源: 题型:
NA代表阿伏加德罗常数,下列说法正确的是( )
A.1 L0.1 mol/L Na2CO3溶液中CO32-和HCO3-总数为0.1 NA
B.22.4L氢气和4g氦气均含有NA个分子
C.含2NA个共价键的CnH2n+2分子的物质的量为2/(3n+l) mol
D.标准状况下,2.24LCl2与稀NaOH溶液反应,转移的电子总数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
环境问题的最终解决要依靠科技进步。下列关于保护生存环境的说法中,不正确的是( )
A.通常利用沉淀反应除去污水中的重金属离子
B.垃圾焚烧不仅可以用于发电,还不会带来任何新的污染
C.减少使用、加强回收和再利用是治理“白色污染”的主要途径
D.可通过改进燃烧装置和燃烧技术,减少煤等化石燃料燃烧产生的污染
查看答案和解析>>
科目: 来源: 题型:
(1)若要配制100mL的0.1mol/LNa2SO4溶液,需称量Na2SO4的质量为多少克?
(2)实验室里常用固体氯化铵与足量熟石灰加热制取氨。若需要2240mL(标准状况)氨,求至少需要氯化铵的质量。
查看答案和解析>>
科目: 来源: 题型:
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式_____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸 B.溴的四氯化碳溶液
C.水 D.酸性高锰酸钾溶液
(3)已知 2CH3CHO+O2 ![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
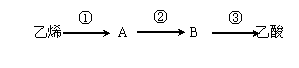 |
反应②的化学方程式为___________________________________,有机物A中的官能团名称 _。
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其结构简式为_______________。
查看答案和解析>>
科目: 来源: 题型:
I、镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:

(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用 ,要使MgSO4完全转化为
沉淀,加入试剂的量应为 。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂②选用 ;写出其反应的离子方程式 。
(4)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为 。
II.关于《必修2》中提到的常见有机物,请回答下列问题:
(1)苯在常温常压下呈 态。
(2)常温常压下气态直链烷烃含碳原子数≤ 。
(3)苯和甲烷中含碳量较高的是 。
(4) 写出苯与浓硝酸、浓硫酸混合液加热反应的化学方程式(用结构简式书写) 。
(5) 写出乙醇和乙酸的酯化反应方程式 。
查看答案和解析>>
科目: 来源: 题型:
第1列
1
①
第2列
第13列
第14列
第15列
第16列
第17列
第18列
2
②
③
④
⑧
3
⑤
⑥
⑦
⑨
(1) 写出元素在周期表中所处位置②:______,画出元素的原子结构示意图③:_ ___
(2) ④⑥⑦元素气态氢化物按稳定性强弱顺序排列:______ __(写氢化物的化学式)。
(3) 将⑥⑦⑨三种元素的最高价氧化物对应水化物按酸性强弱顺序排列:_ (写最高价氧化物对应水化物的化学式)。写出⑤元素单质和水反应的离子方程式:
(4) 用电子式表示CaCl2的形成过程 。
查看答案和解析>>
科目: 来源: 题型:
在KCl、FeCl3、Fe2(SO4)3三种盐配成的混合溶液中,若K+为0.15 mol,Fe3+为0.25 mol,Cl-为0.2 mol,则SO42-为
A.0.1 mol B.0.15 mol C.0.25 mol D.0.35 mol
查看答案和解析>>
科目: 来源: 题型:
已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:
HXO4>H2YO4>H3ZO4。则下列说法不正确的是
A.气态氢化物的稳定性:HX>H2Y>ZH3 B. 非金属活泼性:Z<Y<X
C.单质的氧化性:X2>Y2>Z2 D.原子最外电子层上电子数相等
查看答案和解析>>
科目: 来源: 题型:
山梨酸(CH3—CH=CH—CH=CH—COOH)是一种常用的食品防腐剂。下列关于山梨酸性质的叙述中,不正确的是
A.可与钠反应 B.可与碳酸钠溶液反应
C.可与溴的四氯化碳溶液发生取代反应 D.可生成高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com