
科目: 来源: 题型:
化学平衡常数(K)是化学反应限度的一个重要参数,该常数表示的意义是可逆反应进行的程度,K值越大,表示的意义错误的是( )
A.温度越高 B.反应物浓度越小
C.反应进行的越完全 D.生成物浓度越大
查看答案和解析>>
科目: 来源: 题型:
把 0.05molNaOH 固体分别加入到 100mL 下列液体中,溶液的导电能力变化最小的是( )
A. 自来水 B. 0.05mol/L 盐酸
C. 0.5mol/L 醋酸溶液 D. 0.5mol/L KCl 溶液
查看答案和解析>>
科目: 来源: 题型:
在体积为2L的密闭容器中合成氨,已知在时间t内,氨的物质的量增加了0.6 mol,在此时间内,用H2表示的平均反应速率是0.45mol/(L·s),则t是( )
A.0.44s B.1s C.1.33s D.2s
查看答案和解析>>
科目: 来源: 题型:
下列物质中① NaCl 溶液、② NaOH 、③ H2SO4 、④ Cu 、⑤ CH3COOH 、⑥ NH3·H2O 、 ⑦ CO2 、⑧ 乙醇、⑨ 水, 其中属于电解质的是( )
A. ①②③ B ①②③⑤⑧⑨ C ②③⑤⑥ ⑨ D 全部都是
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应
C.生成物的总焓大于反应物的总焓时,反应吸热,ΔH>0
D.ΔH的大小与热化学方程式的计量系数无关
查看答案和解析>>
科目: 来源: 题型:
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目: 来源: 题型:
Ⅰ. (6分)有机物A的结构简式如图所示:
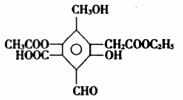
(1)A与过量NaOH完全反应时,A与参加反应的NaOH的物质的量之比为_________________。
(2)A与新制Cu(OH)2完全反应时,其中A与被还原的Cu(OH)2的物质的量之比为_________________。
(3)A与过量的NaHCO3完全反应时,A与参加反应的NaHCO3物质的量之比为_________________。
Ⅱ. (14分)以乙烯为原料可以通过下图所示路线合成E和H(部分反应条件已略去):
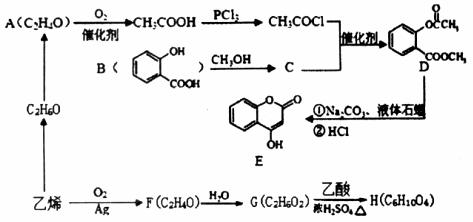
(1)A中含有的官能团名称为_________________。
(2)G和乙酸反应生成H的反应类型为_________________;C转化为D的反应类型是_________________。
(3)写出D与足量NaOH溶液完全反应的化学方程式_________________。
(4)F的结构简式为_________________,H的结构简式为_________________;
(5)写出同时满足下列条件的B的一种同分异构体的结构简式_________________。
A. 能发生银镜反应
B. 核磁共振氢谱只有4个峰
C. 能与FeCl3溶液发生显色反应,水解时每mol可消耗3molNaOH
查看答案和解析>>
科目: 来源: 题型:
Ⅰ. (6分)下列描述中正确的是( )
A. CS2为V形的极性分子
B. ![]() 的空间构型为平面三角形
的空间构型为平面三角形
C. SF6中有6对完全相同的成键电子对
D. SiF4和![]() 的中心原子均为sp3杂化
的中心原子均为sp3杂化
Ⅱ. (14分)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为__________________________________;
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,![]() 和
和![]() 的离子半径分别为69pm和78pm,则熔点NiO_________________FeO(填“<”或“>”);
的离子半径分别为69pm和78pm,则熔点NiO_________________FeO(填“<”或“>”);
(3)NiO晶胞中Ni和O的配位数分别为_________________、_________________;
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为_________________;

(5)丁二酮肟常用于检验![]() :在稀氨水介质中,丁二酮肟与
:在稀氨水介质中,丁二酮肟与![]() 反应可生成鲜红色沉淀,其结构如右上图所示。
反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是_________________。氮镍之间形成的化学键是_________________;
②该结构中,氧氢之间除共价键外还可存在_________________键;
③该结构中,碳原子的杂化轨道类型有_________________。
查看答案和解析>>
科目: 来源: 题型:
Ⅰ. (6分)利用化学原理对工厂排放的废水、废渣等进行有效检测与合理处理。
(1)染料工业排放的废水中含有大量有毒的![]() ,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去
,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去![]() 的离子方程式为__________________________。
的离子方程式为__________________________。
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 |
|
|
|
|
|
|
| 开始沉淀时的pH | 1.9 | 7.0 | — | — | 4.7 | — |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(2)印刷电路铜板腐蚀剂常用FeCl3。腐蚀铜板后的混合浊液中,若![]() 、
、![]() 和
和![]() 的浓度均为
的浓度均为![]() ,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中
,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中![]() 和
和![]() 的实验步骤:①__________;②___________;③过滤。(提供的药品:C12、浓
的实验步骤:①__________;②___________;③过滤。(提供的药品:C12、浓![]() 、NaOH溶液、CuO、Cu)。
、NaOH溶液、CuO、Cu)。
Ⅱ. (14分)下图表示某些化工生产的流程(部分反应条件和产物略去)

(1)反应Ⅰ需在500℃进行,其主要原因是_________________。
(2)G转化为H的过程中,需要不断补充空气,其原因是_________________。
(3)写出反应Ⅲ的化学方程式_________________。
(4)工业上,向析出K的母液中通氨气,加入细小食盐颗粒,冷却后可析出副产品。通入氨气的作用是_________________(填序号)。
a. 增大![]() 的浓度,使J更多地析出
的浓度,使J更多地析出
b. 使K更多地析出
c. 使K转化为M,提高析出的J的纯度
(5)写出上述流程所涉及的化学工业的名称_________________。
查看答案和解析>>
科目: 来源: 题型:
10ml由两种有机物按等物质的量组成的混合气体,该混合气体完全燃烧需17.5ml的O2,并生成15ml的CO2和15ml的水蒸气(所有气体体积均在相同状况下测定)。
试在下表中填出所有可能组合(有多少填多少,不一定填满)。
| 第1组(两种有机物结构简式) | 第2组(两种有机物结构简式) | 第3组(两种有机物结构简式) | 第4组(两种有机物结构简式) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com