
科目: 来源: 题型:
下列事实中能充分说明苯分子的平面正六边形结构中,不含有一般的碳碳双键和
碳碳单键的是
A.苯的一元取代物只有一种结构 B.苯的邻位二元取代物只有一种结构
C.苯的间位二元取代物无同分异构体 D.苯的对位二元取代物无同分异构体
查看答案和解析>>
科目: 来源: 题型:
下列物质进行一氯取代反应后,只能生成四种沸点不同产物的是
A.(CH3)2CHCH2CH2CH3 B.(CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2 D.(CH3)3CCH2CH3
查看答案和解析>>
科目: 来源: 题型:
Ⅰ. (6分)有机物A的结构简式如图所示:

(1)A与过量NaOH完全反应时,A与参加反应的NaOH的物质的量之比为_________________。
(2)A与新制Cu(OH)2完全反应时,其中A与被还原的Cu(OH)2的物质的量之比为_________________。
(3)A与过量的NaHCO3完全反应时,A与参加反应的NaHCO3物质的量之比为_________________。
Ⅱ. (14分)以乙烯为原料可以通过下图所示路线合成E和H(部分反应条件已略去):

(1)A中含有的官能团名称为_________________。
(2)G和乙酸反应生成H的反应类型为_________________;C转化为D的反应类型是_________________。
(3)写出D与足量NaOH溶液完全反应的化学方程式_________________。
(4)F的结构简式为_________________,H的结构简式为_________________;
(5)写出同时满足下列条件的B的一种同分异构体的结构简式_________________。
A. 能发生银镜反应
B. 核磁共振氢谱只有4个峰
C. 能与FeCl3溶液发生显色反应,水解时每mol可消耗3molNaOH
查看答案和解析>>
科目: 来源: 题型:
Ⅰ. (6分)下列描述中正确的是( )
A. CS2为V形的极性分子
B. ![]() 的空间构型为平面三角形
的空间构型为平面三角形
C. SF6中有6对完全相同的成键电子对
D. SiF4和![]() 的中心原子均为sp3杂化
的中心原子均为sp3杂化
Ⅱ. (14分)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为__________________________________;
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,![]() 和
和![]() 的离子半径分别为69pm和78pm,则熔点NiO_________________FeO(填“<”或“>”);
的离子半径分别为69pm和78pm,则熔点NiO_________________FeO(填“<”或“>”);
(3)NiO晶胞中Ni和O的配位数分别为_________________、_________________;
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为_________________;

(5)丁二酮肟常用于检验![]() :在稀氨水介质中,丁二酮肟与
:在稀氨水介质中,丁二酮肟与![]() 反应可生成鲜红色沉淀,其结构如右上图所示。
反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是_________________。氮镍之间形成的化学键是_________________;
②该结构中,氧氢之间除共价键外还可存在_________________键;
③该结构中,碳原子的杂化轨道类型有_________________。
查看答案和解析>>
科目: 来源: 题型:
Ⅰ. (6分)利用化学原理对工厂排放的废水、废渣等进行有效检测与合理处理。
(1)染料工业排放的废水中含有大量有毒的![]() ,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去
,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去![]() 的离子方程式为__________________________。
的离子方程式为__________________________。
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 |
|
|
|
|
|
|
| 开始沉淀时的pH | 1.9 | 7.0 | — | — | 4.7 | — |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(2)印刷电路铜板腐蚀剂常用FeCl3。腐蚀铜板后的混合浊液中,若![]() 、
、![]() 和
和![]() 的浓度均为
的浓度均为![]() ,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中
,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中![]() 和
和![]() 的实验步骤:①__________;②___________;③过滤。(提供的药品:C12、浓
的实验步骤:①__________;②___________;③过滤。(提供的药品:C12、浓![]() 、NaOH溶液、CuO、Cu)。
、NaOH溶液、CuO、Cu)。
Ⅱ. (14分)下图表示某些化工生产的流程(部分反应条件和产物略去)

(1)反应Ⅰ需在500℃进行,其主要原因是_________________。
(2)G转化为H的过程中,需要不断补充空气,其原因是_________________。
(3)写出反应Ⅲ的化学方程式_________________。
(4)工业上,向析出K的母液中通氨气,加入细小食盐颗粒,冷却后可析出副产品。通入氨气的作用是_________________(填序号)。
a. 增大![]() 的浓度,使J更多地析出
的浓度,使J更多地析出
b. 使K更多地析出
c. 使K转化为M,提高析出的J的纯度
(5)写出上述流程所涉及的化学工业的名称_________________。
查看答案和解析>>
科目: 来源: 题型:
10ml由两种有机物按等物质的量组成的混合气体,该混合气体完全燃烧需17.5ml的O2,并生成15ml的CO2和15ml的水蒸气(所有气体体积均在相同状况下测定)。
试在下表中填出所有可能组合(有多少填多少,不一定填满)。
| 第1组(两种有机物结构简式) | 第2组(两种有机物结构简式) | 第3组(两种有机物结构简式) | 第4组(两种有机物结构简式) |
查看答案和解析>>
科目: 来源: 题型:
Ⅰ. 在实验室利用下列装置,可制备某些气体并验证其化学性质。

完成下列表格:
| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| (1) | 乙烯 | _________________ | _________________ |
| (2) | 乙炔 | A→C→E | _________________ |
Ⅱ. 某学习小组设计实验测定电石样品的纯度。
经查阅有关资料得知H2S、PH3能与硫酸铜溶液反应,相关仪器和药品装置图如下:

(1)按气体从左到右的流向选择最佳的装置组合是(选填字母序号):_________
(2)为保证测定的精度,要求产生乙炔的气流较为平缓,在分液漏斗中应装入的液体是________________。
(3)若电石样品的质量为m1g,F吸收乙炔前后的质量差为m2g,则电石样品中CaC2质量分数![]() =_______________。
=_______________。
查看答案和解析>>
科目: 来源: 题型:
氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一。
(1)传统哈伯法合成氨工艺中相关的反应式为:![]()
![]()
![]()
![]() 。
。
①该反应的平衡常数K的表达式为:K=_________。升高温度,K值________(填“增大”“减小”或“不变”)。
②不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2的起始物质的量之比为1:3)。分析表中数据,__________(填温度和压强)时H2转化率最高,实际工业生产不选用该条件的主要原因是________________。
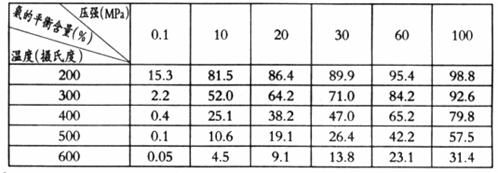
③下列关于合成氨说法正确是___________(填字母)
A. 使用催化剂可以提高氮气的转化率
B. 寻找常温下的合适催化剂是未来研究的方向
C. 由于△H<0、△S>0,故合成氨反应一定能自发进行
(2)最近美国Simons等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法。它既有液氢燃料电池的优点,又克服了液氢不易保存的不足。其装置为用铂黑作为电极,加入电解质溶液中,一个电极通人空气,另一电极通入氨气。其电池反应为
![]()
你认为电解质溶液应显______性(填“酸性”、“中性”、“碱性”),写出负极电极反应式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com